细胞膜包覆、靶向小胶质细胞、具有多种类酶活性的超小纳米探针,通过清除脑部活性氧调控小胶质细胞表型,缓解脑部氧化应激及改善炎症环境。
实验方法概要:
**通过超小Cu2−xSe纳米颗粒表面的Cu2+离子络合槲皮素(简写为CSPQ纳米颗粒),赋予纳米颗粒类过氧化氢酶(CAT)、类过氧化物酶(POD)和类超氧化物歧化酶(SOD)的性质,实现优于单一槲皮素和单一Cu2−xSe纳米颗粒的ROS清除能力。更优的多种类酶活性使CSPQ纳米颗粒具有**的抗炎作用,可以将小胶质细胞极化为具有神经保护作用的M2表型。
其次,我们采用神经元细胞(MES23.5细胞)的细胞膜包覆CSPQ,赋予其**的靶向小胶质细胞的性能,并揭示**靶向性能是由于神经元细胞膜表面的血管内皮细胞黏附分子VCAM-1和小胶质细胞表面的整合素α4β1之间的特异性相互作用。最后,我们利用聚焦超声打开血脑屏障将超小纳米颗粒**递送至脑部、改善氧化应激和炎症反应,**提高帕金森模型小鼠的学习和认知功能。
图文解析
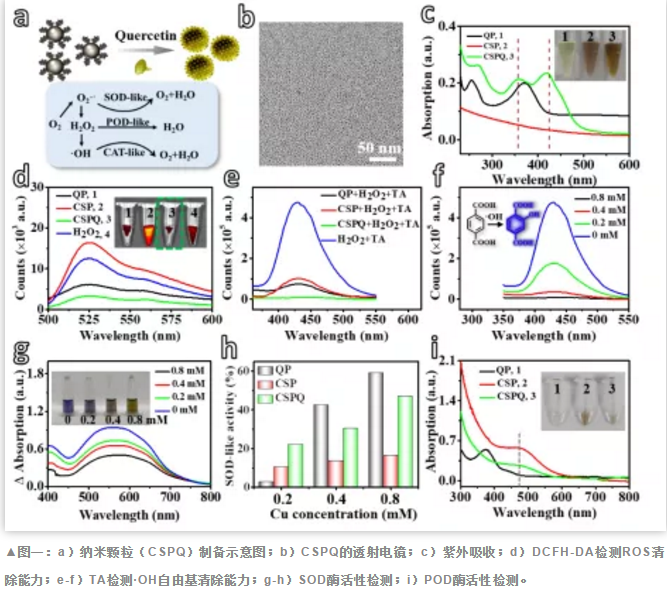
如图一所示,我们利用超小Cu2-xSe纳米颗粒表面的Cu2+离子络合槲皮素,制备了具有**清除ROS能力的CSPQ纳米颗粒,其清除能力优于单纯的槲皮素(QP)和Cu2-xSe纳米颗粒(CSP)。酶活性检测试剂盒证明所得CSPQ纳米颗粒通过多种类酶活性(CAT、SOD、 POD酶)清除ROS。
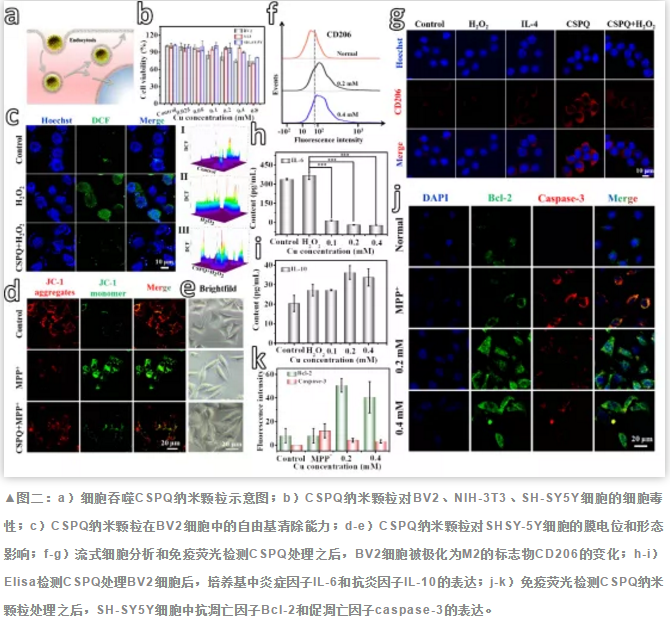
如图二所示,我们检测了CSPQ纳米颗粒对细胞微环境的调控作用,以及对细胞的保护作用机制。CSPQ纳米颗粒被吞入细胞后,对BV2和3T3、以及SH-SY5Y细胞均表现出较低的毒性,并且可以**清除小胶质细胞BV2中的ROS,明显改善SH-SY5Y细胞的膜电位和形态。利用流式分析和免疫荧光方法,我们发现CSPQ纳米颗粒可以将小胶质细胞BV2极化为对神经具有保护作用的M2表型,**促炎因子IL-6的释放,同时促进抗炎因子IL-10的释放。纳米颗粒还使SH-SY5Y细胞的抗凋亡因子Bcl-2表达上调,促凋亡因子caspase-3表达下调。
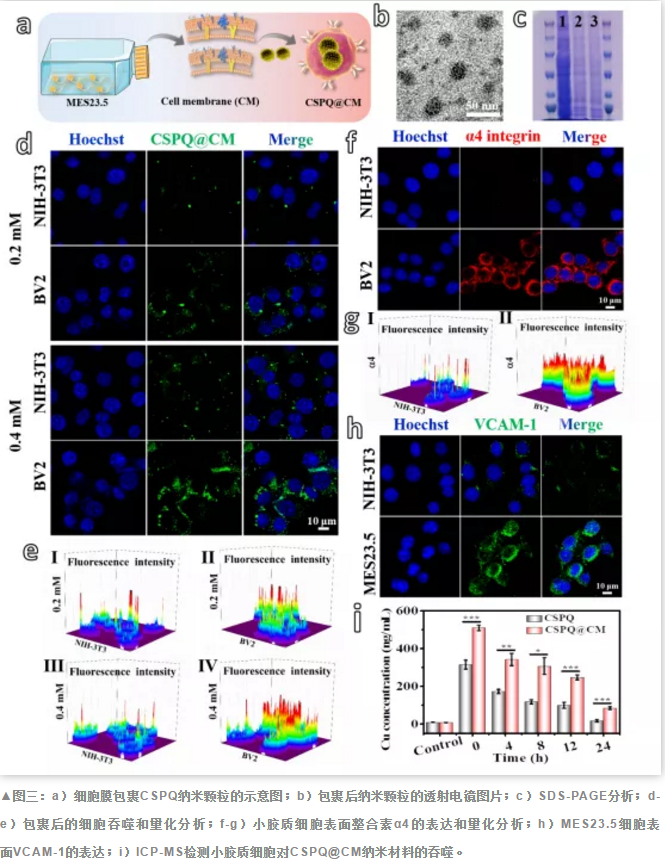
如图三所示,为了提高CSPQ纳米颗粒的递送效率和效果,我们提取神经元细胞MES23.5的细胞膜,包覆CSPQ纳米颗粒。发现细胞膜包裹明显增加了小胶质细胞对CSPQ纳米颗粒的吞噬,具有**的靶向性,其靶向作用是由于小胶质细胞表面高表达的整合素α4β1与神经元细胞MES23.5表面的血管细胞黏附分子VCAM-1之间的特异性相互作用。
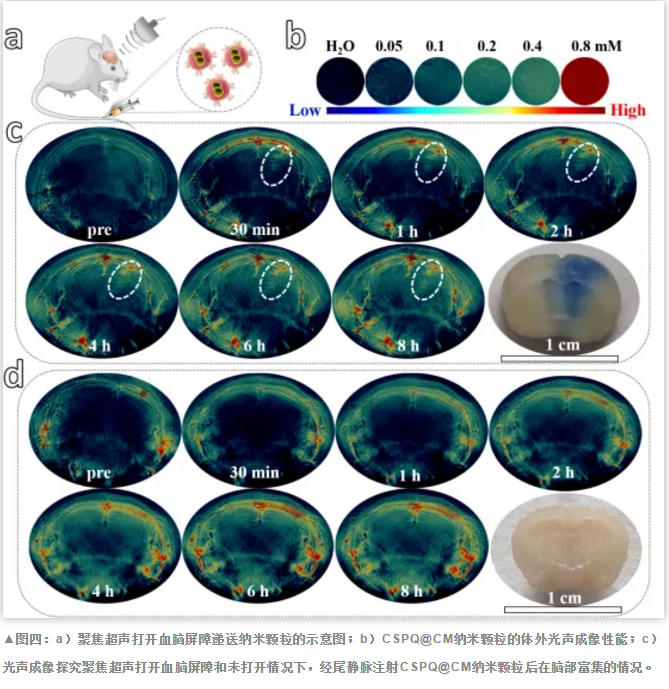
由于Cu2-xSe纳米颗粒在近红外区具有很强的表面等离子体共振吸收,可以**地将近红外光转化为热实现光声成像,因此,我们利用光声成像监测CSPQ@CM纳米颗粒在脑部的富集效果,发现与没有聚焦超声相比,采用聚焦超声打开血脑屏障可以**提高纳米颗粒在脑部的富集量(如图四所示)。
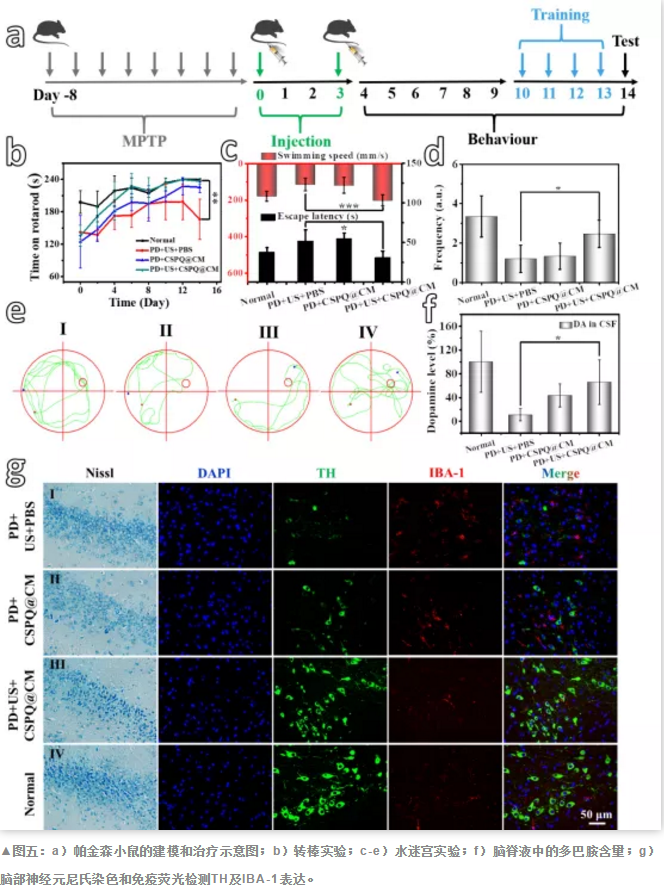
我们通过两次尾静脉注射CSPQ@CM纳米颗粒**帕金森小鼠(如图五所示)。**之后的小鼠在转棒实验中,停留在转棒上的时间明显增加。在水迷宫实验中,游泳速度得到提升,能够快速找到逃生平台。在空间探索实验中,**组小鼠的记忆认知也得到明显改善,穿过逃生平台的次数明显增多。此外,我们利用Elisa检测不同组小鼠的脑脊液中多巴胺含量,发现经过**的小鼠脑脊液中多巴胺含量增加。脑部组织的尼氏染色、TH、IBA-1免疫荧光显示,CSPQ@CM纳米颗粒可以**改善帕金森小鼠脑部微环境,提高帕金森病的**效果。




 齐岳微信公众号
齐岳微信公众号 官方微信
官方微信 库存查询
库存查询