菲(PHE)由于其非凡的性能,在许多领域(如染料、农药和光电材料等)都得到了研究和应用。但是,对于菲的分离一直以来都面临较大的困难。目前,工业上使用的优选技术是结晶、蒸馏、区域熔化和制备色谱。然而,这些方法是能源密集型的,并且对环境不友好。因此,制定节能和实用的方法能将PHE从其芳香族异构体蒽(ANT)混合物中分离出来**重要。这里,介绍了一种基于水溶性大环的主客体化学来实现PHE的分离方法。
水溶性大环化合物通过在水中的疏水相互作用而具有将疏水客体分子封装在其空腔中的能力。为了实现水溶性大环化合物实现PHE和ANT的分离,大环化合物的空腔尺寸应该与PHE的尺寸相匹配。此外,为了在封装后释放客体,大环应该具有刺激响应性。而在各种刺激中,光可以以、无创和清洁的方式远程控制分子的封装和释放。并且考虑到偶氮苯(azo)基团由于E↔Z光异构化特性而在光响应材料中具有广泛的应用,可以考虑引入作为大环的骨架以赋予大环光响应性并扩大大环腔体的尺寸
与以前报道的从ANT中分离PHE的策略相反,这里报道的方法利用了聚阳离子水溶性偶氮基大环1的主客体络合特性,在环境温度下,通过固液萃取实现了从ANT中分离PHE。
之后,为了实现E,E-1从芳族异构体混合物中的选择性分离PHE,我们研究了主体E,E-1和客体(ANT或PHE)之间的相互作用。核磁共振氢谱显示,E,E-1上的质子的信号(H2-6)向低场移动(Fig.1a,b),表明E,E-1和ANT之间存在弱相互作用。但是对于ANT上质子的信号几乎察觉不到,这归因于ANT的低水溶性。此外,通过核磁共振氢谱(Fig.2,b和c)表征了E,E-1和PHE之间的主客体络合作用。E,E-1上质子的信号(H1-6)向低场移动,PHE上质子的信号显现,表明E,E-1对PHE的溶解有促进作用。我们进而通过核磁滴定实验确定了E,E-1•PHE和E,E-1•ANT的化学计量比均为1:1,且利用公式实际分离测量了水中E,E-1•PHE和E,E-1•ANT之间的缔合常数,分别为4.5×104 M-1和6.7×104 M-1。紧接着,为了研究水中的络合选择性,我们通过向E-1的水溶液中加入1.00 eq的PHE和1.00 eq的ANT进行竞争实验(Fig.2d)。核磁共振氢谱结果与E,E-1·PHE的核磁共振氢谱基本一致。因此,我们推断E,E-1在水中可以选择性地与PHE结合。
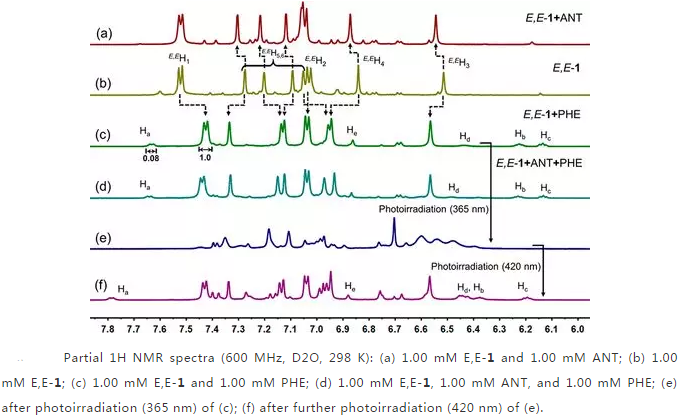
然而,1的空腔尺寸在E,E-1 →Z,Z-1光异构化后**减小,因此要考虑客体PHE的包封和释放是否可以被光控制。E,E-1·PHE经紫外光(365 nm)照射后,发生1的E→Z光异构化,PHE上的质子信号(Ha-e)从核磁共振氢谱中消失(Fig.2e),证明了PHE的释放。然后在可见光(420 nm)的照射后,Ha-e质子信号的出现表明PHE被再次封装在E,E-1的腔中(Fig.2f)。
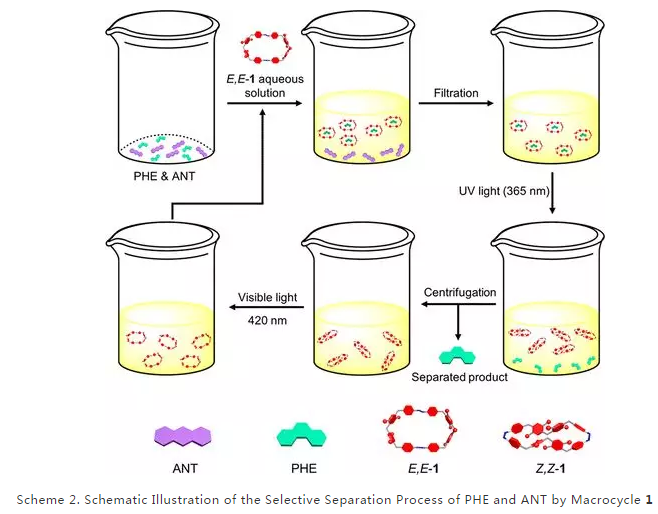
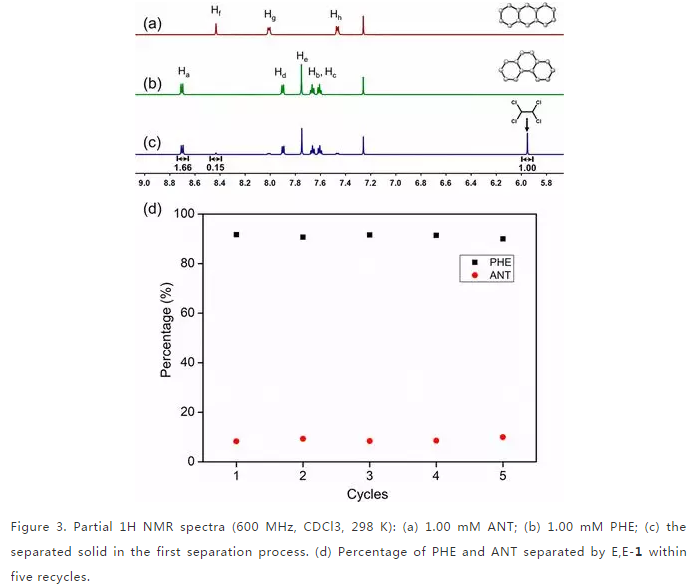
我们在研究了1在水中的光异构化行为和主客体络合作用后,利用1从PHE和ANT的混合物中选择性的分离PHE。其分离过程如图(Scheme 2)所示。分离结果通过核磁共振氢谱进行表征,显示其主要信号与PHE质子有关(Fig.3a-c),并且PHE的纯度为91.7%。此外,大环1可以重复使用至少5次,而且不会明显降低PHE的分离性能(Fig.3d),五次结果PHE的平均纯度为91.1%。
负载紫杉醇CSNRDARRC-PCL-PGA/TPGS多肽纳米颗粒
葫芦脲[7]包载超分子金纳米簇(CB[7]/FGGC-AuNCs
葫芦[7]脲(CB[7])修饰聚(N-异丙基丙烯酰胺)(PNIPAM)
金刚烷-聚丙烯酸/β环糊精的支化聚乙烯亚胺(PAA‑AD/PEI‑βCD)
温馨提示:西安齐岳生物科技有限公司供应的产品仅用于科研,不能用于其他用途




 齐岳微信公众号
齐岳微信公众号 官方微信
官方微信 库存查询
库存查询