今天西安齐岳生物的小编zhn分享缓释注射剂中不同载体系统(微球、⽔凝胶、脂质体)适用场景,这其实取决于药物性质、给药途径、释放时长以及组织相容性。下面整理一份清晰的对比和应用场景分析:
1、微球(Microspheres / Polymer-based particles)
特点:
一般用可降解高分子如 PLGA、PCL 等制备。
通过控制聚合物类型、分子量、乳化方式,可精确调控药物释放时间(几天到几个月)。
药物多为小分子、蛋白或多肽。
可注射或植入组织内(常见肌内注射)。
适用场景:
情况 | 微球是否适合 | 原因 |
需要长期缓释(周-月) | ✅ | 聚合物降解慢,可稳定释放 |
药物为水溶性蛋白/多肽 | ✅/⚠️ | 可以包封,但可能存在初始爆发释放(burst release)问题 |
局部给药(肌肉、皮下) | ✅ | 可形成沉积,缓慢降解 |
靶向特定器官 | ⚠️ | 一般非靶向,需要表面修饰或复合其他载体 |
典型应用:
糖尿病长效胰岛素(PLGA微球)
长效药物注射剂
药物缓释疫苗

2、水凝胶(Hydrogel)
特点:
高含水量三维网络,可吸水膨胀。
药物分子通过物理包埋或化学键结合,可控释放。
可以响应环境刺激(pH、温度、酶等)。
生物相容性好,注射后可原位凝胶。
适用场景:
情况 | 水凝胶是否适合 | 原因 |
药物为蛋白、抗体、干细胞 | ✅ | 高含水量,保护生物活性 |
需要局部缓释 | ✅ | 可原位注射成凝胶,局部停留 |
对释放时间要求不长(天-周) | ✅ | 高分子交联度可调,释放相对较快 |
靶向深部组织或大体积填充 | ✅ | 可形成可注射的填充体 |
典型应用:
关节腔注射用缓释药
局部肿瘤药物递送(原位凝胶)
干细胞载体或组织工程支架
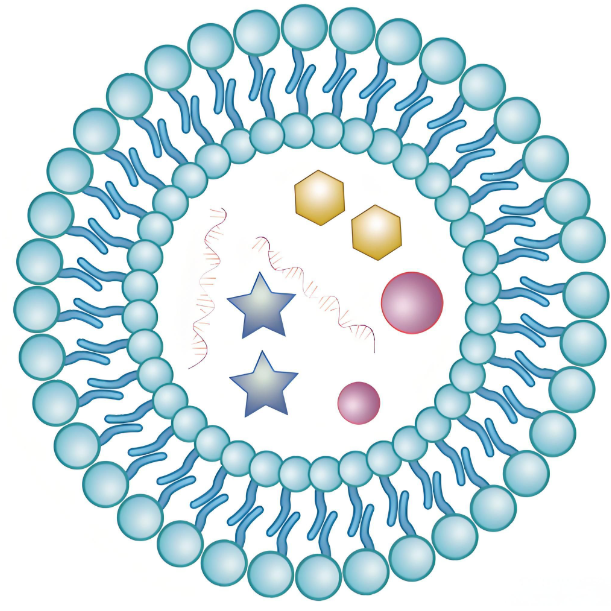
3、脂质体(Liposomes / Lipid nanoparticles)
特点:
脂质双层包裹水溶性药物,疏水药物可嵌入脂质膜。
易生物降解,血液相容性好。
可通过表面修饰实现靶向。
释放时间短至中等(小时-几天),长效需要改良(PEG化、固体脂质等)。
适用场景:
情况 | 脂质体是否适合 | 原因 |
药物为小分子疏水性药物 | ✅ | 可嵌入脂质膜,保护稳定性 |
靶向给药(如肿瘤、肝脏) | ✅ | 可通过PEG化或配体修饰延长循环/靶向 |
需要短至中等缓释(数小时-数天) | ✅ | 脂质体膜可控制药物缓释速率 |
对生物活性要求高的蛋白/核酸 | ✅ | 可封装核酸、蛋白,但长效缓释不易 |
典型应用:
Doxil(PEGylated多柔比星脂质体)
LNP mRNA疫苗(短期血液缓释和细胞递送)
脂溶性激素或维生素缓释注射剂
总结对比
特性 | 微球 | 水凝胶 | 脂质体 |
释放周期 | 中-长(周-月) | 短-中(天-周) | 短-中(小时-数天) |
药物类型 | 小分子/蛋白/多肽 | 蛋白/抗体/细胞 | 小分子、蛋白、核酸 |
给药方式 | 肌内/皮下注射或植入 | 原位注射/局部 | 静脉、局部注射 |
生物活性保护 | 中等 | 高 | 高 |
靶向能力 | 需改性 | 可局部控制 | 可表面修饰实现靶向 |
优势 | 长效、可控 | 高生物相容性、保护生物活性 | 可靶向、保护药物、可调释速率 |
缺点 | 初期爆发释放、制备复杂 | 长期稳定性一般、体积膨胀 | 缓释时间受限、易被吞噬 |
设计原则小提示:
如果追求 几周到几个月的长期缓释 → 选微球(PLGA 等)。
如果是 短期局部缓释、蛋白或细胞载体 → 选水凝胶。
如果是 需要保护药物活性、可通过血液给药、短中期缓释 → 选脂质体。
西安齐岳生物提供不同载体系统(微球、⽔凝胶、脂质体),如有需求,可联系我们定制合成




 齐岳微信公众号
齐岳微信公众号 官方微信
官方微信 库存查询
库存查询