小分子交联剂对于探测生物分子间的相互作用和在处理大型蛋白复合物和内在无序蛋白时的交联质谱(CXMS)是非常宝贵的。现有的化学交联剂只针对一小部分氨基酸残基,限制了交联的数量和类型,而传统的光交联剂几乎不选择性地针对所有残基,使数据分析变得复杂。
设计合成了基于光保护的喹酮甲基化(PQM)的一系列交联剂,能够通过的Michael加成靶向9个亲核残基。除了Asp、Glu、Lys、Ser、Thr和Tyr外,PQM交联剂还**地交联了Gln、Arg和Asn,**,这些化学交联剂还不能作为靶点,用单一交联剂**地增加了靶点残基的数量。
设计了一种含NHS酯基和光保护ortho-QM(o-QM)的双功能交联剂NHQM。邻硝基苄基在酚羟基上的邻位甲基上连接了两个氟原子,当加入到蛋白中时,NHS会很快和暴露的Lys残基反应,将光保护的o-QM放置在相互作用蛋白的残基旁边,o-硝基苄基在紫外线照射下被清除,生成o-QM,并与附近的亲核侧链发生交联。
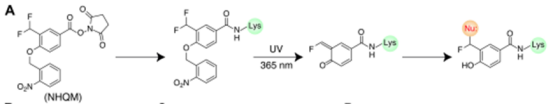
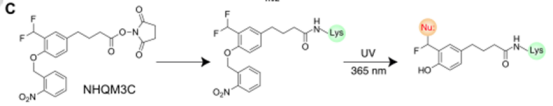
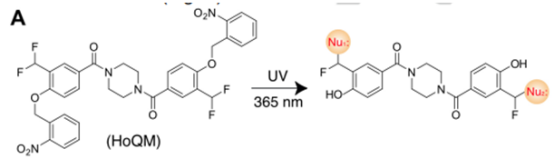
为了增加交联剂的灵活性,还合成了NHQM3C,在NHQM的spacer 中添加了三个亚甲基。实验结果表明,NHQM和NHQM3C用小分子交联剂将自然残基的靶标库扩大到9个亲核残基。为了使细胞内**的交联成为可能,还设计了一个具有同功能的交联剂HoQM,在两端都采用了光保护的o-QM。将NHS酯替换为光保护的QM可以在光激活前消除交联剂的化学反应性,从而使其进入细胞而不会引起细胞毒性。此外,两端的QM可以增加交联类型的多样性,因为QM与NHS酯相比会和更多的残基反应。
与DNA交联的试剂仍然很少,因为大多数交联剂的反应更倾向于蛋白-蛋白而不是蛋白-DNA交联。甲醛是主要的试剂交联试剂,但只能和在2埃以内的蛋白发生交联。QM能**地烷基化脱氧核苷,因此,推断NHQM应该能够使蛋白质与DNA交联,实验证明假设是正确的。
总之,这些PQM交联剂的光活化和多靶点反应性将大大增强蛋白质-蛋白质、蛋白质- DNA网络研究和结构生物学研究的化学交联基础技术。
更多技术资料及其相关产品了解,可浏览官网首页分栏。




 齐岳微信公众号
齐岳微信公众号 官方微信
官方微信 库存查询
库存查询