一文介绍RhCl3三氯化铑作用下小分子肽与硼酸的反应活性
发布时间:2020-11-09 作者:axc 分享到:
Rh(III)盐参与的有机金属生物偶联反应:酪氨酸残基发生金属化形成Rh(III)/酪氨酸配合物,并同时与硼酸试剂转金属化引入官能化的芳基片段,该复合物又可以在强还原剂二硫苏糖醇(DTT)作用下分解为氨基酸残基。他们利用这种方法实现了多肽和蛋白质在水溶液介质中温和的生物偶联,同时还可引入其他重要的官能团,如亲和基团或荧光基团。基于无机连接体的亚稳定性,偶联产物仅在亲核性的氧化还原物种存在时才会被切断,对**的生物环境较为稳定。
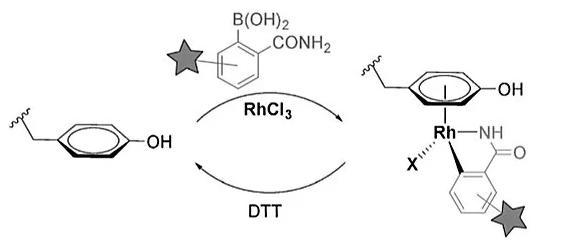
考察不同过渡金属盐对硼酸转化的反应活性,以炔烃官能化的芳基硼酸对酪氨酸残基进行修饰,使用“化学”蛋白质印迹分析的方法确定引入硼酸基团的效果。仅有两种金属盐能参与配位炔烃标记的蛋白质:一种是先前报道的铜(II)盐参与的反应,另一种涉及Rh(III)参与的过程,简单的RhCl3盐便可作为的金属促进剂。
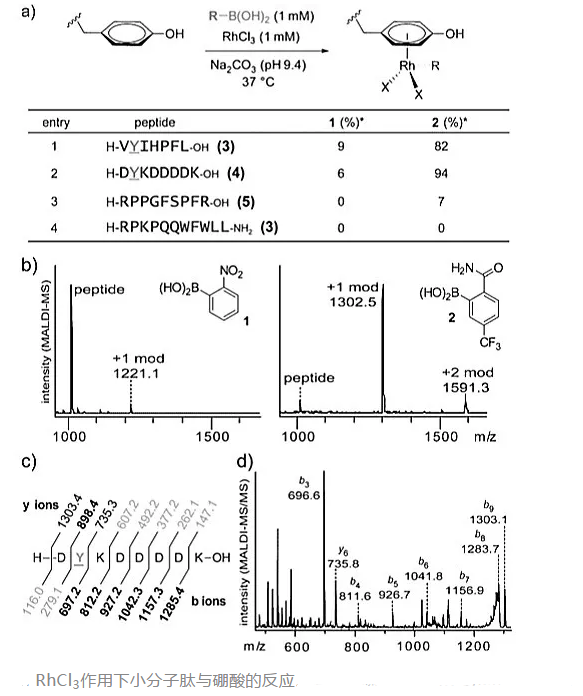
通过小分子肽设计的实验确定了酪氨酸残基是成功实现修饰过程的充要条件。以RhCl3对四种小分子肽进行修饰,以Na2CO3溶液作为缓冲体系,在37 ℃的反应温度下反应18 h,邻位含有酰胺基且间位含有三氟甲基的苯硼酸2表现出比邻硝基苯硼酸1更好的反应活性。由于H-RPPGFSPFR-OH与H-RPKPQQWFWLL-NH2中没有酪氨酸残基,小分子肽未表现出明显的反应活性。利用质谱分析考察生成产物的比例,以分子离子峰及碎片峰的信息确定了酪氨酸残基是有机金属修饰的位点。
以上资料来自互联网,如有侵权,请联系我们进行删除
仅用于科研




 齐岳微信公众号
齐岳微信公众号 官方微信
官方微信 库存查询
库存查询