DSPE-PEG-NHS怎么连接抗体?
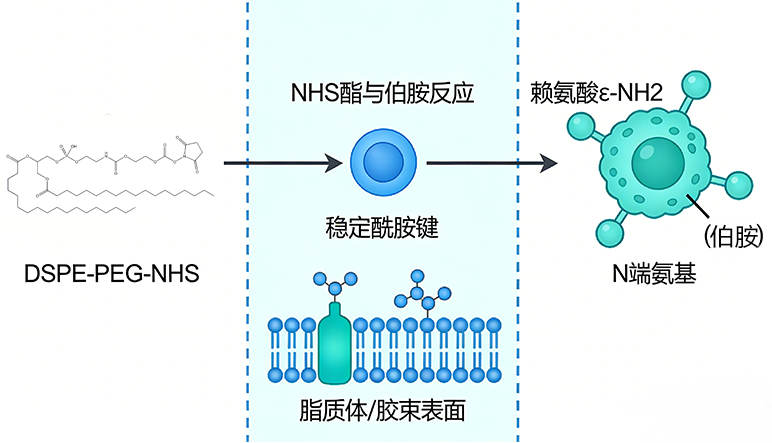
DSPE-PEG-NHS连抗体,本质上是用 NHS 酯和抗体表面的伯胺(主要是赖氨酸 ε-NH2、少量N端氨基)反应,形成稳定酰胺键。这类反应常用于把抗体接到脂质体/胶束表面。
常用做法如下:
1)先处理抗体
把抗体换到不含伯胺的缓冲液里,例如 PBS、HEPES、磷酸盐缓冲液。
不要用 Tris、glycine、乙醇胺 这类含胺缓冲液,也尽量避免 BSA、明胶等含蛋白稳定剂,因为它们会和 NHS 竞争,明显降低偶联效率。
2)现配 DSPE-PEG-NHS
DSPE-PEG-NHS 对水分和碱性条件比较敏感,很容易水解失活,所以要临用前现配。通常先溶于少量 DMSO / DMF / 乙醇 / 氯仿 等,再尽快加到反应体系里;不用时应低温、干燥保存。
3)进行偶联反应
把 DSPE-PEG-NHS 加入抗体溶液中,在中性到弱碱性条件下反应。
对蛋白/抗体,实操上通常用 pH 7.2–8.0 的无胺缓冲液;而 DSPE-PEG-NHS 的 NHS 端在 pH 8–10 也能高效与伯胺反应。为了兼顾抗体稳定性,常优先选 pH 7.4–8.0。
可直接按下面这个研究/开发常用窗口起步:
抗体浓度:1–10 mg/mL
DSPE-PEG-NHS : 抗体摩尔比:先试 10:1、20:1、30:1 三档
反应时间:1–4 h,室温,避光、轻轻混匀
BroadPharm 给出的通用 PEG-NHS 标记条件中,20 倍摩尔过量常可给 IgG 引入约 4–6 个 PEG linker/抗体。
4)封闭未反应的 NHS
反应结束后,用 glycine 或 Tris 封闭残余 NHS,避免后续继续乱反应。文献中有直接加 glycine 终止反应的做法。
5)纯化
用 透析、超滤或脱盐柱 去除游离的 DSPE-PEG-NHS、DMSO/DMF 和小分子副产物。PEG-NHS 抗体偶联后的纯化,文献和通用协议里都常用透析或脱盐柱。
6)再插入脂质体
如果你的目标是做抗体修饰脂质体,常见路线不是“先成脂质体再直接拿抗体去碰”,而是:
先做 DSPE-PEG-抗体偶联物 → 再通过 post-insertion 后插入到预制脂质体中。
相关研究指出,DSPE-PEG-NHS 应尽量在干膜后尽快直接与抗体反应,这样可减少 NHS 水解,提高偶联收率。
一个可直接起步的小试方案
适合做 DSPE-PEG2000/3400-NHS 偶联 IgG:
抗体换液到 PBS,pH 7.4,去掉 Tris/glycine/BSA。
DSPE-PEG-NHS 临用前溶于少量无水 DMSO。
缓慢加入抗体溶液,使有机相占比尽量低。
设 10:1、20:1、30:1 三组摩尔比,室温反应 2 h。
加 glycine 终止 10–20 min。
超滤/脱盐纯化。
如果做靶向脂质体,再与含 mPEG-DSPE 的胶束或预制脂质体进行 post-insertion。
这个流程符合 NHS-胺偶联的一般规则,也和 DSPE-PEG-NHS 在脂质体后插入体系中的公开做法一致。
你需要注意的坑
第一,缓冲液错了。 Tris、glycine 常见,直接抢反应。
第二,DSPE-PEG-NHS放久了。 NHS 很容易水解,尤其高温、偏碱、见水后更明显,所以一定现配现用。
第三,抗体取向不可控。 NHS 主要打赖氨酸,属于随机偶联;抗体上可修饰位点很多,靠近结合区时可能影响活性和亲和力,产物也会更异质。若你特别在意抗体活性/朝向,通常会考虑 maleimide-巯基、糖基位点或其他定点偶联路线。
怎么判断连上了
常见确认方法有:
SEC / FPLC:看游离抗体和偶联物分离
SDS-PAGE:条带轻微上移/拖尾
BCA/UV:测蛋白保留量
脂质体体系:测粒径、PDI、zeta、电镜、抗体密度
功能验证:ELISA / cell binding / flow cytometry
这些属于常规表征思路;真正关键的是最后的抗原结合活性有没有保住。




 齐岳微信公众号
齐岳微信公众号 官方微信
官方微信 库存查询
库存查询