多刺激响应型 MOF 纳米载体载药定制合成技术服务
一、多刺激响应型 MOF 纳米载体载药系统研究综述
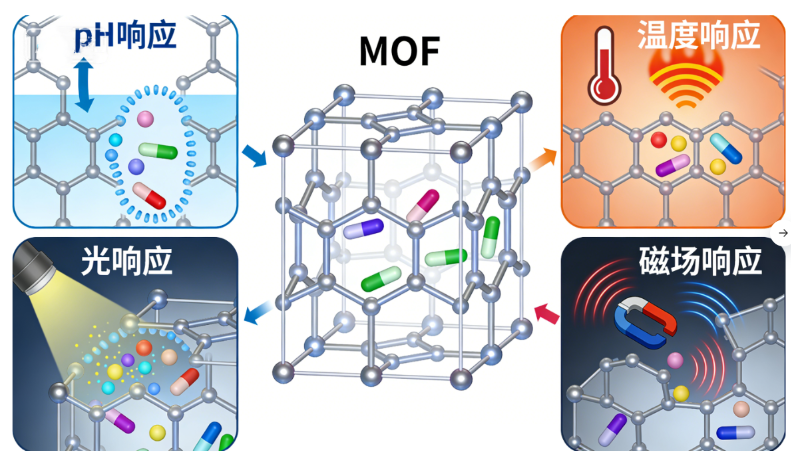
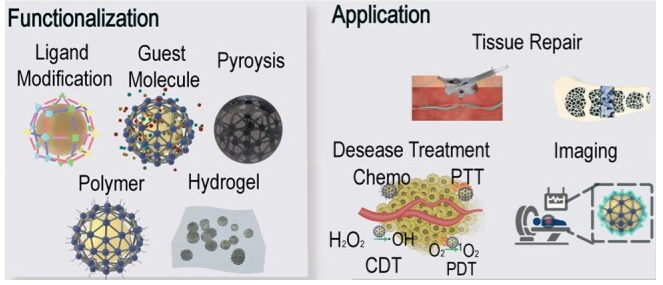
金属有机框架(Metal-Organic Frameworks, MOFs)是一类由金属离子 / 簇与有机配体通过配位键自组装形成的晶态多孔材料,凭借其可设计的孔道结构、很高的比表面积、多样的功能位点等特性,成为纳米载药领域的研究热点。传统 MOF 载药体系存在药物释放缺乏靶向性与可控性的弊端,西安齐岳生物可以提供对多刺激响应型 MOF 纳米载体的修饰,通过对多终MOF骨架(如锆基 MOF(UiO-66 系列),铁基 MOF(MIL-88 系列),锌基 MOF(ZIF-8/ZIF-67),镧系 MOF(Eu-MOF/Tb-MOF)等)进行功能化修饰,可实现对pH、温度、氧化还原、酶、光、磁场等多种内 / 外源性刺激的精准响应,在肿瘤、炎症等疾病的靶向治疗中展现出独特优势。
二、西安齐岳生物多刺激响应型 MOF 纳米载体载药定制服务内容
定制服务核心方向
西安齐岳生物依托的配位合成平台与功能修饰技术,可提供多维度、定制化的多刺激响应型 MOF 纳米载体载药合成服务,具体细分方向如下:
1、响应类型定制
pH-氧化还原双响应型:
针对肿瘤微环境(弱酸性、高谷胱甘肽浓度)设计,通过在 MOF 骨架中引入酸敏配位键(如亚胺键、腙键)和二硫键交联的有机配体,实现载体在肿瘤部位的精准降解与药物释放,适配化疗药物的靶向递送。
温度-酶双响应型:
结合热敏聚合物(如聚 N - 异丙基丙烯酰胺)修饰与酶切位点(如基质金属蛋白酶 MMP-2/MMP-9 识别序列)功能化,适用于温热治疗与酶表达异常疾病的联合治疗。
光-磁场双响应型:
通过掺杂光敏剂(如卟啉、酞菁)与磁性纳米颗粒(如 Fe₃O₄),实现光控药物释放与磁靶向定位的协同,可用于影像引导下的精准给药。
多联响应型:
支持 pH - 氧化还原 - 酶、光 - 温度 - 磁场等三联及以上响应机制的定制,满足复杂疾病治疗的个性化需求。
2、MOF 基体材料定制
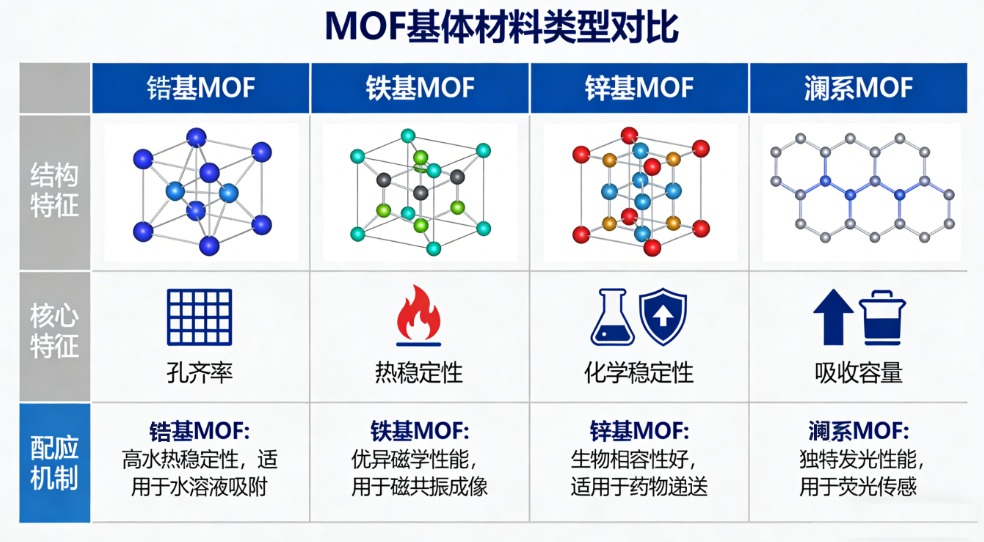
可根据载药需求与响应机制,定制不同基体的 MOF 材料,具体包括:
| MOF 基体类型 | 核心特性 | 适配响应机制 |
| 锆基 MOF(UiO-66 系列) | 化学稳定性强、孔道可调,易引入功能基团 | pH - 氧化还原双响应、酶响应 |
| 铁基 MOF(MIL-88 系列) | 生物相容性好、可磁响应,降解产物可参与铁代谢 | 磁场 - 酸响应、光热 - 载药协同 |
| 锌基 MOF(ZIF-8/ZIF-67) | 酸敏性强、制备工艺简便,易于表面修饰 | pH 响应、pH - 氧化还原双响应 |
| 镧系 MOF(Eu-MOF/Tb-MOF) | 具备荧光特性,可实现示踪 - 载药一体化 | 光响应、荧光示踪 - 多刺激释药协同 |
3、适配药物范围
西安齐岳生物可实现多种类型药物的负载定制,涵盖化学药、生物药等不同剂型,具体包括:
化疗类药物:阿霉素(DOX)、紫杉醇(PTX)、顺铂、5 - 氟尿嘧啶(5-FU)、甲氨蝶呤(MTX)等,可通过孔道包埋、表面吸附或配位键偶联实现负载。
靶向类药物:曲妥珠单抗、贝伐珠单抗等单克隆抗体,索拉非尼、厄洛替尼等小分子靶向药,通过点击化学(如 DBCO-NHS)实现与 MOF 载体的定向偶联。
光动力 / 光热治疗药物:卟啉、酞菁、吲哚菁绿(ICG)、IR780 等光敏 / 光热剂,可掺杂于 MOF 骨架或修饰于载体表面,实现诊疗一体化。
基因类药物:siRNA、miRNA、质粒 DNA(pDNA)等,通过静电吸附或阳离子聚合物(如 PEI)介导的功能化实现负载,适配基因 - 化疗联合治疗。
天然活性药物:姜黄素、紫杉醇、青蒿素衍生物等,可利用 MOF 的疏水孔道实现高效包封,提升药物稳定性与生物利用度。
4、药物负载定制方案
针对不同药物的理化性质与给药需求,提供三种核心负载定制工艺,具体如下表所示:
| 负载工艺 | 技术原理 | 适配药物类型 | 负载效率范围 | 核心优势 |
| 孔道包埋法 | 利用 MOF 多孔结构的吸附与包合作用,通过浸渍 - 透析法实现药物负载 | 小分子化疗药、光敏剂 | 60%-90% | 操作简便、药物活性保留度高 |
| 表面偶联法 | 通过 MOF 表面修饰的活性基团(-NH₂、-COOH、-N₃)与药物官能团的共价偶联(如酰胺化、点击化学) | 抗体、多肽、基因药物 | 75%-95% | 靶向性强、药物不易泄漏 |
| 配位掺杂法 | 将药物作为配体或金属离子的配位调节剂,参与 MOF 骨架的自组装过程 | 含配位基团的药物(如顺铂、含羟基 / 氨基的天然药) | 80%-98% | 负载量高、释放可控性强 |
三、定制服务案例展示
西安齐岳生物已完成多例多刺激响应型 MOF 纳米载体载药定制项目,以下为典型案例的图文解析:
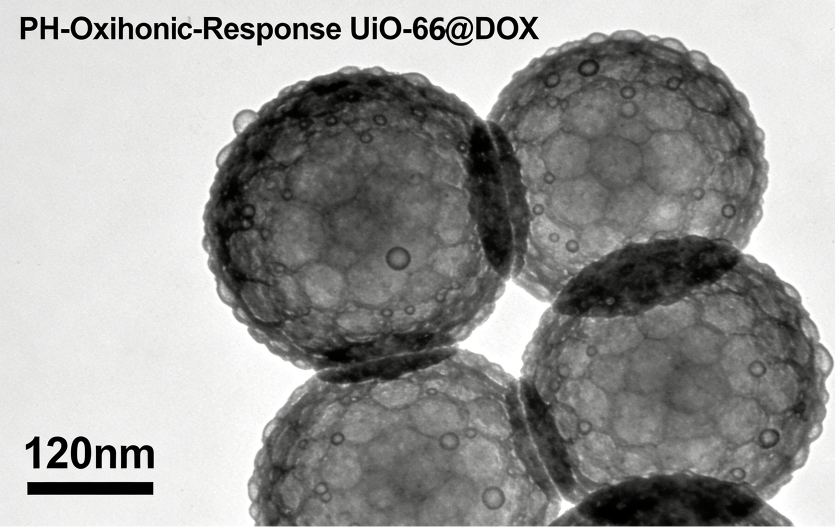
| 案例 1:pH-氧化还原双响应 UiO-66@DOX 载药纳米粒定制 1、定制需求 某生物医药企业需定制用于乳腺癌靶向治疗的 pH - 氧化还原双响应载药 MOF。 2、表征结果与数据 形貌表征:透射电镜(TEM)显示载体呈均一球形,粒径集中在 120nm 左右,分散性良好;
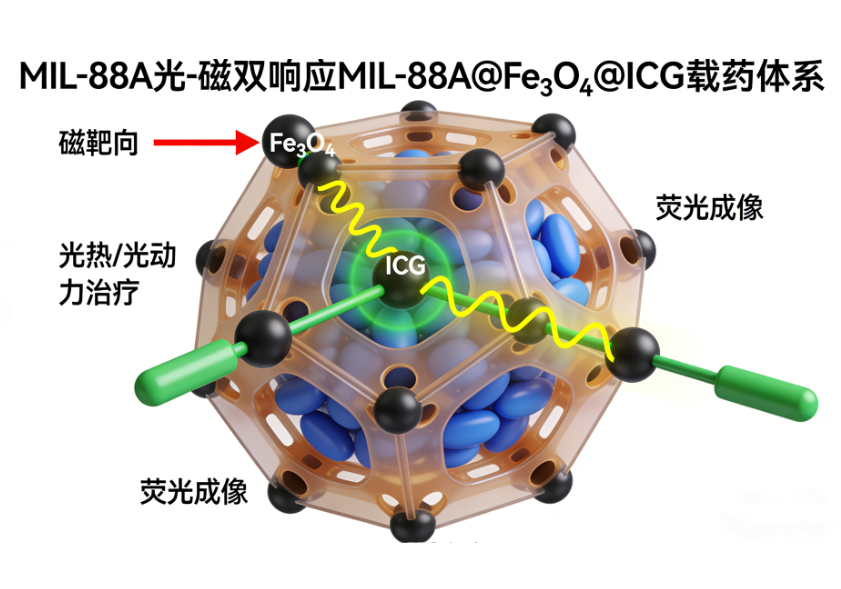
负载效率:通过高效液相色谱(HPLC)检测,阿霉素总负载量达 18.2%,满足定制需求; 响应释放性能:在 pH 7.4(生理环境)下 24h 药物释放率仅 12.5%,而在 pH 5.5+10mM GSH(肿瘤微环境)下 24h 释放率达 85.3%,实现了靶向可控释放 | 案例 2:光 - 磁双响应 MIL-88A@Fe₃O₄@ICG 载药体系定制 1、定制需求 某高校实验室需定制诊疗一体化 MOF 载药系统,要求兼具磁靶向定位、近红外光控释药与荧光成像功能,用于肝癌的联合治疗研究。 2、核心参数与效果 结构设计:以 MIL-88A 为基体,原位掺杂 Fe₃O₄磁性颗粒(实现磁靶向),表面修饰 ICG(光热 / 光动力治疗 + 荧光成像),并包载化疗药索拉非尼; 成像性能:在近红外激发下,载体可发出稳定荧光信号,实现体内外示踪; 治疗协同性:在外加磁场引导下,载体可富集于肝癌部位,经 808nm 激光照射后,实现光热升温(局部温度达 45℃以上)与药物同步释放,体外细胞实验显示对肝癌细胞的抑制率较单一化疗提升 42%。
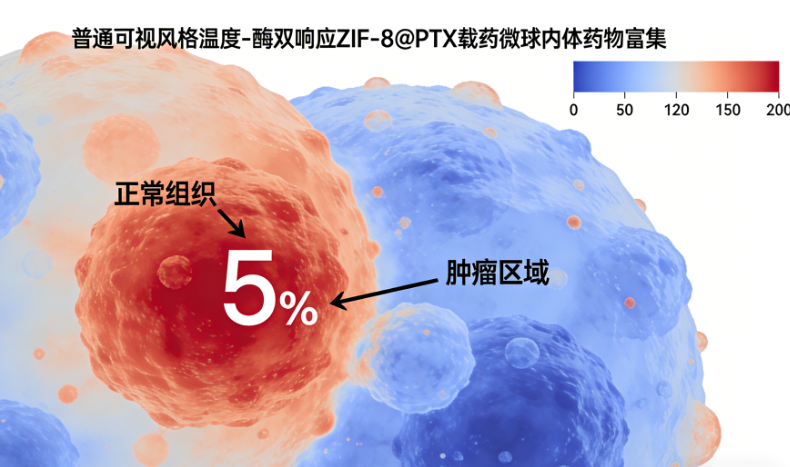
| 3、温度 - 酶双响应 ZIF-8@PTX 载药微球定制 定制亮点 针对胰腺癌(高表达 MMP-9、适宜温热治疗)的治疗需求,在 ZIF-8 表面接枝热敏 PNIPAM 聚合物与 MMP-9 酶切肽段,包载紫杉醇。体内实验显示,该载体经 42℃温热刺激 + 肿瘤部位 MMP-9 酶切后,药物在病灶部位的富集浓度较普通 ZIF-8@PTX 提升 5 倍,且对正常胰腺组织的毒副作用显著降低。
|
四、多刺激响应型 MOF 纳米载体定制的技术优势
西安齐岳生物在多刺激响应型 MOF 纳米载体定制领域,具备定制灵活、响应精准、性能优异、适配多元四大核心技术优势,技术实力对标国际前沿,可满足多场景应用需求:
1. 模块化定制,适配多元需求搭建通用型 MOF 纳米平台,通过金属配体交换实现 “即插即用” 式定制。针对肿瘤治疗可定制 Cu/Fe 基多模式协同治疗载体,针对炎症疾病可切换为 Ce 基 ROS 清除与 pH 响应载体,无需频繁重构载体骨架,大幅提升定制效率。
2. 多刺激精准响应,靶向递送可控载体可实现 pH、氧化还原、温度、微波等多重刺激协同响应,且响应阈值可精准调控。肿瘤微环境下能同步识别酸性 pH 与高浓度 GSH 实现药物靶向释放;农药递送场景中,Ag-TCPP@MPN 载体可依环境 pH 实现 52.6%-80.0% 梯度控释,还可实现微波 - 谷胱甘肽双响应以应对耐药肿瘤。
3. 高负载 + 优生物相容性,兼顾疗效与安全依托 MOF 很高比表面积,载体药物负载率可达 38% 以上(如噻苯咪唑负载量 38.14%),远超传统纳米载体;优选 ZIF-8、UiO-66 等基体,降解产物无明显细胞毒性,可安全代谢,规避体内蓄积与免疫风险。
4. 动态分子设计,拓展响应维度引入可移动有机基团与柔性连接体,实现压力、粘度、电场等特殊刺激响应。工业催化场景可通过压力调控孔道开合,生物传感领域能借电场响应提升检测灵敏度,拓展载体应用边界。
五、相关参考文献
文献一、基于金属-有机框架系统的可逆多级刺激响应性和多色室温磷光到荧光的转变
原文链接:https://doi.org/10.1016/j.cej.2025.160075
英文名:Reversible multilevel stimuli-responsiveness and multicolor roomtemperature phosphorescence to fluorescence transition based on ametal-organic framework system
主要内容:
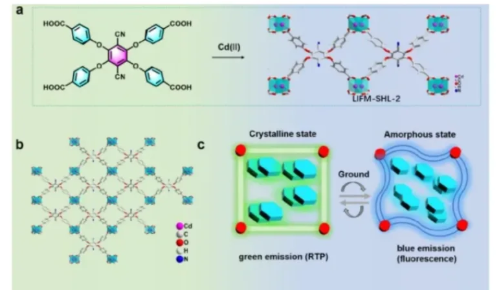
提出了一种名为LIFM-SHL-2的MOF,它表现出多级刺激响应性,可以通过研磨或盐酸(HCl)蒸气熏蒸在高效绿色RTP和蓝色荧光之间转变。由于其扭曲的分子结构和多孔结构,LIFM-SHL-2的RTP发射容易被外部刺激改变,导致相变和独特的多级响应。LIFM-SHL-2从晶体到非晶态的机械诱导转变可以恢复初始晶体的弹性框架特性,从而导致可变发光。
文献二、酸响应性Fe/Mn双金属有机框架纳米系统FeMn@R@H,用于细胞焦亡和增强免疫治疗
英文名:An acid-responsive MOF nanomedicine for augmented anti-tumor immunotherapy via a metal ion interference-mediated pyroptotic pathway
链接:https://www.sciencedirect.com/science/article/abs/pii/S0142961223003411
主要内容:
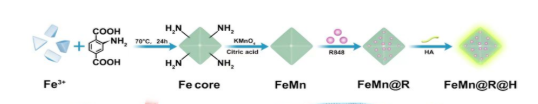
设计了一种负载金属离子和免疫佐剂R848的酸响应性Fe/Mn双金属有机框架纳米系统FeMn@R@H,用于将细胞焦亡和增强免疫疗法相结合。在肿瘤酸性微环境的作用下,FeMn@R@H 被触发分解并释放 Fe3+和 Mn2+离子,从而引发芬顿样反应产生 ROS诱导细胞焦亡。一方面,焦亡引起的细胞破裂会诱导肿瘤细胞释放促炎细胞因子和免疫原性成分,进一步导致免疫原性细胞死亡,促进*肿瘤免疫反应。另一方面,共递送的R848可以通过激活TLR7/8途径逆转免疫抑制性肿瘤微环。总之,这种肿瘤特异性治疗系统可以将金属离子和R848共递送至肿瘤组织,以实现焦亡介导的程序性细胞死亡和增强的*肿瘤免疫治疗。
文献三、用于生物医学的功能性金属有机框架的研究进展
英文名:Recent progress in functional metal-organic frameworks for bio-medical application
链接:DOI:https://doi.org/10.1093/rb/rbad115
主要内容:
Ren等人所证明的那样,直接浸泡法可用于使用小客体分子对MOFs进行功能化。利用溶剂热合成工艺将两种常用的小分子药物多柔比星和塞来昔布负载到IRMOF-3上。如图所示,这种复合材料与传统的注射水凝胶结合使用时,在pH响应性、*肿瘤疗效、生物相容性以及在口腔肿瘤部位同时释放疏水性和亲水性药物等方面,都是一种很有前景的局部治疗口腔癌的载体。
六、相关产品:
| 产品名称 | 核心特性 | 适用场景 | 关键参数 / 优势 |
| Cu/Fe 基多模式协同治疗 MOF 纳米载体 | pH / 氧化还原双响应,整合光热、化学动力与化疗等协同作用 | 肿瘤综合治疗 | 适配肿瘤微环境低 pH、高 GSH 特征,精准释放药物;光热治疗效率达 29.3±0.8%,羟基自由基产率 0.18±0.01μM/min,可降低肿瘤耐药性 |
| β-CD-nMOF@MTX 纳米载体 | Zn 基骨架,pH / 谷胱甘肽双响应,表面修饰 β- 环糊精 | 乳腺癌靶向化疗 | 载药率达 66.67%,包封率 90.92%;仅在肿瘤微环境(pH5.5+10mM GSH)中释放米托蒽醌,肿瘤抑制率 69.57%,大幅降低药物心脏毒性 |
| Ce-UIO-66 MOF 纳米载体 | Ce 基配位结构,兼具 pH 响应与 ROS 清除能力 | 炎症性疾病干预、催化氧化 | 纯度 98% 以上,粒径 50 - 200nm,热分解温度超 400℃;Ce⁴⁺/Ce²⁺的氧化还原特性可清除炎症部位过量活性氧,同时实现药物精准释放 |
| Ag-TCPP@MPN MOF 纳米载体 | pH 响应,金属多酚网络增强粘附性 | 农药靶向递送(如作物病害防治) | 依环境 pH(4.96 - 8.5)实现 52.6% - 80.0% 梯度控释,降低农药残留至 0.05mg/Kg;提升载体在作物表面保留时间,减少雨水冲刷损失 |
| BIS@ZIF - 8 纳米农药载体 | pH / 紫外光双响应,ZIF - 8 骨架保障生物安全性 | 农业智能除草 | 粒径 118.46nm,载药量 14.86%;稗草叶片保留率达 76.26%,抗雨水冲刷能力强,紫外光下释放速率显著提升,除草效果优于纯除草剂,对非靶标生物无毒 |
| MnMOF 微波 - 谷胱甘肽双响应纳米载体 | Mn 基骨架,微波与谷胱甘肽协同响应 | 耐药肿瘤热动力化疗 | 可应对微波耐药肿瘤,通过微波触发热效应,搭配谷胱甘肽响应释放药物,实现热疗与化疗协同,提升耐药肿瘤治疗效果 |




 齐岳微信公众号
齐岳微信公众号 官方微信
官方微信 库存查询
库存查询