西安齐岳生物提供的PLGA载药载荧光定制合成服务手册
一、综述
聚乳酸-羟基乙酸共聚物(PLGA)作为一种具有良好生物相容性、生物可降解性及无毒性的高分子材料,被广泛应用于药物递送系统的构建。其降解产物乳酸和羟基乙酸可参与人体代谢循环,最终以二氧化碳和水的形式排出体外,有效降低了药物递送过程中的生物安全性风险。PLGA载药系统能够实现药物的控释、缓释,提升药物靶向性,减少药物副作用;而载荧光功能的引入,则为药物在体内外的分布、代谢及作用机制研究提供了可视化手段。基于此,PLGA载药载荧光定制合成已成为生物医药领域药物研发、临床前研究的重要支撑技术,西安齐岳生物依托多年高分子材料合成经验与药物递送系统研发实力,推出全方位的PLGA载药载荧光定制合成服务,满足不同科研与应用需求。
二、西安齐岳生物PLGA载药载荧光定制合成服务详情
1、定制服务核心细分方向
西安齐岳生物围绕PLGA载药载荧光定制,构建了涵盖“基础载药定制”“载荧光定制”“载药-载荧光双功能定制”“靶向修饰载药/荧光定制”四大核心细分方向的服务体系,各方向精准匹配不同科研诉求:
| 种类 | 具体服务 |
| 1、基础载药定制 | 专注于单一药物的PLGA载体包封,核心目标是实现药物的高效负载与可控释放,根据药物性质优化载体粒径、形貌及降解速率。 |
| 2、载荧光定制 | 通过物理包埋或化学偶联方式将荧光分子引入PLGA载体,实现载体的可视化追踪,可根据追踪需求选择不同激发/发射波长的荧光分子。 |
| 3、载药-载荧光双功能定制 | 整合载药与载荧光功能,既能实现药物的靶向递送与控释,又可通过荧光信号实时追踪药物递送过程,为药物作用机制研究提供一体化解决方案。 |
| 4、靶向修饰载药/荧光定制 | 在PLGA载药/载荧光载体表面修饰靶向分子(如抗体、多肽、适配体、叶酸等),提升载体对特定细胞或组织的靶向识别能力,降低脱靶效应。 |
2、可负载药物类型
西安齐岳生物可针对不同理化性质的药物开展PLGA负载定制,涵盖小分子化学药物、大分子生物药物等多个类别,具体可负载药物包括但不限于:
| 种类 | 具体产品 |
| 1、小分子化疗药物 | 阿霉素、紫杉醇、多西他赛、顺铂、5-氟尿嘧啶、甲氨蝶呤、喜树碱、长春瑞滨等 |
| 2、光动力治疗药物 | 二氢卟吩e6(Ce6)、血卟啉单甲醚(HMME)、卟啉衍生物等 |
| 3、抗炎药物 | 蛋白质类药物(胰岛素、生长因子、抗体片段)、多肽类药物(亮丙瑞林、生长抑素)、核酸类药物(siRNA、miRNA、DNA疫苗)等; |
| 4、大分子药物 | 在PLGA载药/载荧光载体表面修饰靶向分子(如抗体、多肽、适配体、叶酸等),提升载体对特定细胞或组织的靶向识别能力,降低脱靶效应 |
| 5、其他特殊药物 | 中药活性成分(如姜黄素、丹参酮、人参皂苷)、光敏剂、抗氧化剂等 |
3、PLGA载药载荧光定制服务汇总表
| 定制方向 | 可负载药物/荧光分子 | 核心负载方法 | 关键可定制参数 | 适用场景 |
| 基础载药定制 | 小分子化疗药、抗炎药、中药活性成分等 | 乳化-溶剂挥发法、纳米沉淀法、物理吸附法 | 粒径(50nm-5μm)、形貌(球形/棒状)、包封率(≥60%)、释放曲线 | 药物控释研究、体外细胞药效学实验 |
| 载荧光定制 | Ce6、FITC、Rhodamine B、Cy3、Cy5、量子点等 | 物理包埋法、化学偶联法 | 荧光分子种类、荧光强度、粒径均一性、光稳定性 | 载体体内外分布追踪、细胞摄取实验 |
| 载药-载荧光双功能定制 | 化疗药+荧光分子、光敏剂+荧光分子、中药成分+荧光分子等 | 双乳化法、共沉淀法、分步负载法 | 药物包封率、荧光量子产率、粒径分布、释放与追踪同步性 | 药物递送机制研究、靶向治疗疗效评估 |
| 靶向修饰载药/荧光定制 | 药物/荧光分子+靶向分子(抗体、多肽、叶酸、适配体等) | 化学偶联法+负载法、表面修饰后负载法 | 靶向分子修饰密度、靶向结合力、载药效率、体内靶向性 | 肿瘤靶向治疗研究、组织特异性药物递送实验 |
4、药物负载定制方法及工艺优化
西安齐岳生物根据药物的溶解性、稳定性及靶向需求,采用多种成熟的负载方法,并提供全程工艺优化服务,确保负载效率与载体性能:
• 乳化-溶剂挥发法(W/O/W、O/W):适用于水溶性药物、脂溶性药物及大分子药物的负载,通过调控乳化剂种类与浓度、有机相比例、搅拌速率等参数,优化载体粒径分布(50nm-5μm可调)与药物包封率;
• 纳米沉淀法(溶剂置换法):适用于脂溶性药物的负载,工艺简单、温和,可制备粒径均一的纳米级PLGA载药颗粒,避免药物因高温或强剪切力失活;
• 物理吸附法:适用于对溶剂敏感的大分子药物(如蛋白质、核酸),通过载体表面电荷相互作用或疏水作用实现药物吸附,很大限度保留药物生物活性;
• 化学偶联法:针对需要长期稳定负载或靶向修饰的药物,通过共价键将药物与PLGA载体连接,提升载药稳定性,减少药物突释;
• 工艺优化要点:根据客户需求优化载体形貌(球形、棒状、纳米纤维等)、表面电荷(Zeta电位可调)、降解速率(通过PLGA乳酸/羟基乙酸比例调控,比例50:50-90:10)、药物释放曲线(缓释、控释、脉冲释放)等关键参数。
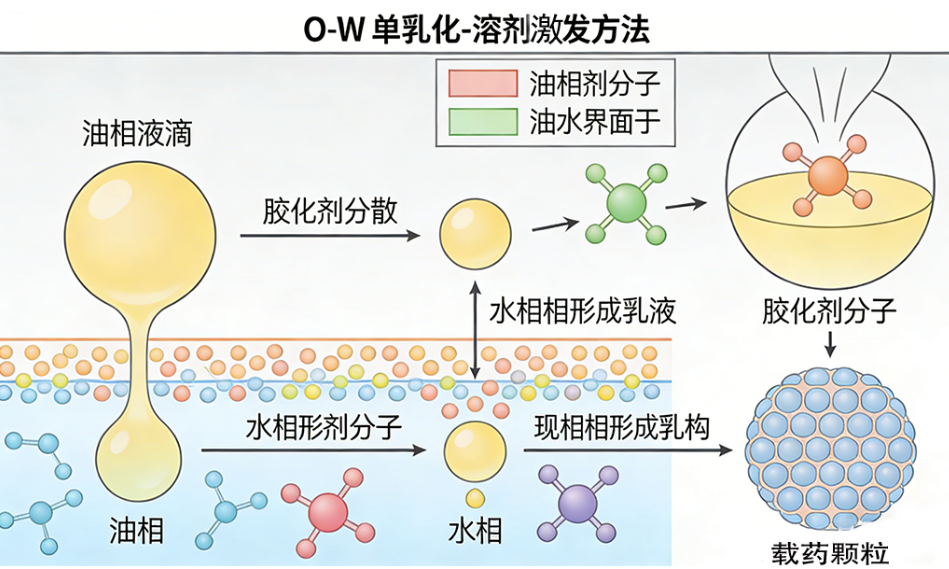
三、PLGA载药载荧光定制案例(图文展示)
案例一:PLGA载药阿霉素(PLGA/DOX)定制合成 1. 定制需求 客户需求:制备PLGA载阿霉素纳米颗粒,要求粒径100-200nm,包封率≥70%,实现pH响应型药物释放,用于肿瘤细胞靶向化疗研究。 2.定制方案及工艺 采用W/O/W双重乳化-溶剂挥发法制备 3.表征结果
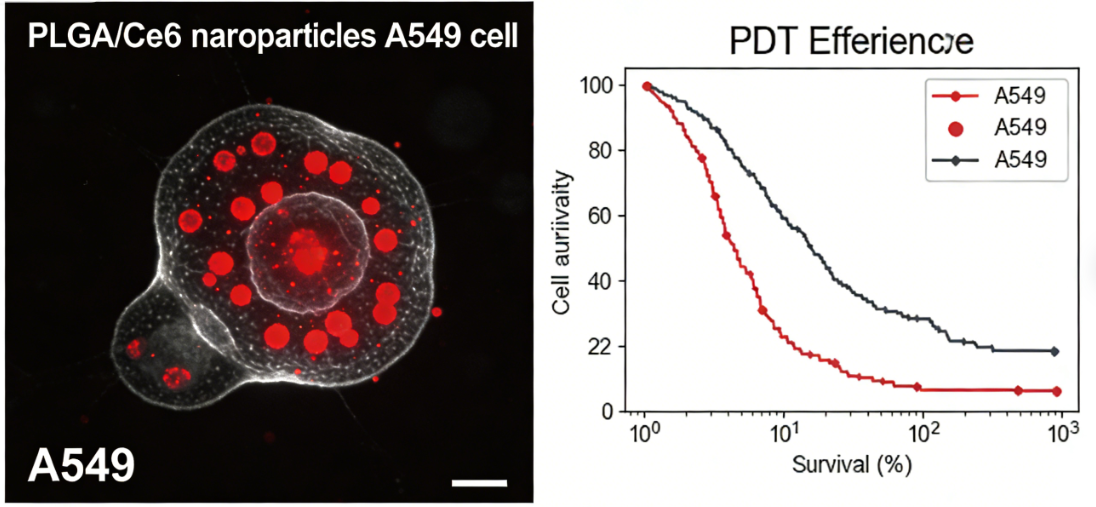
| 案例二:PLGA载荧光二氢卟吩e6(PLGA/Ce6)定制合成 1.定制需求 客户需求:制备PLGA载荧光二氢卟吩e6(Ce6)纳米颗粒,要求粒径50-100nm,荧光强度稳定,Ce6包封率≥80%,用于光动力治疗(PDT)及治疗过程可视化追踪。 2.定制方案及工艺 采用纳米沉淀法(溶剂置换法)制备 3.表征结果
|
四、PLGA载药载荧光定制合成技术优势
西安齐岳生物凭借多年技术积累与研发经验,在PLGA载药载荧光定制合成领域形成多维度技术优势,具体如下:
1、高安全可调控:采用 FDA 批准 PLGA 原料,LA/GA 比例、分子量可控,降解产物可代谢,生物相容性优异。
2、多工艺广负载:掌握乳化 - 溶剂挥发等多种制备工艺,适配小分子、大分子药物及荧光分子的负载需求。
3、高精度强定制:精准调控载体粒径、形貌、表面电荷,可定制缓释、控释或响应型释放曲线,批间差异小。
4、靶向可视化协同:表面可修饰靶向分子实现主动靶向,荧光标记稳定,支持体内外载体分布与药物释放追踪。
5、定制服务全支持:按需定制专属方案,提供从工艺设计到样品表征的全流程技术支持,适配小试、中试规模。
五、PLGA载药载荧光相关文献分享
文献一、中文名:可NIR-II荧光成像的多功能化疗栓塞微球PLGA@Re-DOX的制备及其在肝癌荧光手术导航中的应用
英文名:Preparation and Application of Multifunctional PLGA@Re-DOX Chemoembolization Microspheres with NIR-II Fluorescence Imaging for HCC Fluorescence-guided Surgery
链接:http://xdswyxjz.cnjournals.com/xdswyxjz/ch/reader/download_pdf.aspx?falg=1&file_no=202418003&quarter_id=18&year_id=2024
主要内容:
本研究旨在开发具备近红外二区(NIR-II)荧光成像性能的多功能化疗栓塞微球,评估其在肝癌NIR-II荧光手术导航中的应用效果。研究制备了NaGdF4:Nd@NaGdF4纳米颗粒(Re NPs)和PLGA基微球,通过透射电子显微镜、荧光光谱仪等手段表征了Re NPs的形貌和荧光性能,以及PLGA基微球的形貌、元素组成。利用紫外光谱仪测定了PLGA微球对阿霉素(DOX)的装载和释放情况,并通过CCK-8实验和溶血实验评估其生物相容性。结果显示,Re NPs具有良好的单分散性和均一球形结构,具备优异的NIR-II荧光成像性能;PLGA及PLGA@Re-DOX微球尺寸均一,生物相容性良好,DOX包封率可达2.5%且能缓慢释放。体内实验表明,PLGA@Re-DOX微球经肝动脉递送后,NIR-II荧光成像可清晰显示肿瘤边缘,有望实现肝癌的NIR-II荧光成像和荧光手术导航。
文献二、中文名:用于肺部给药的荧光PLGA纳米载体:表面电荷的影响
英文名:Fluorescent PLGA Nanocarriers for Pulmonary Administration: Influence of the Surface Charge
链接:https://diposit.ub.edu/dspace/bitstream/2445/209229/1/Fluorescent%20PLGA%20Nanocarriers%20for%20Pulmonary%20Administration_Pharmaceutics.pdf
主要内容:
针对呼吸道疾病治疗中药物肺部分布不均、全身副作用大等问题,本研究制备了负载Cy5红色荧光素的PLGA纳米胶囊(Cy5/PLGA),分为正电荷(Cy5/PLGA+)和负电荷(Cy5/PLGA-)两种类型,探讨其表面电荷对肺部给药效果的影响。研究表征了纳米胶囊的胶体稳定性、细胞毒性,并评估了其在两种肺相关细胞(巨噬细胞和肺泡上皮细胞)中的摄取效率,同时通过气管内滴注进行了体内滞留实验。结果显示,两种纳米胶囊在培养介质和生物介质中均具有优异的胶体稳定性,冷冻储存后稳定性良好,且在高达10 mg/ml的浓度下对肺细胞无细胞毒性。细胞摄取实验表明,阴离子纳米胶囊的摄取速度更快、摄取量更高(在巨噬细胞中高10倍,在肺泡上皮细胞中高2.5倍);体内实验显示,阴离子PLGA纳米胶囊经气管内滴注1小时后可保留在所有肺叶中,24小时后聚集在肺巨噬细胞中,是一种具有显著转化潜力的肺部免疫调节递送系统。
文献三、中文名:荧光成像功能化聚乳酸-羟基乙酸共聚物的制备及应用
英文名:Fluorescence Imaging Enabled Poly(Lactide-Co-Glycolide)
链接:https://b-real.lab.westlake.edu.cn/PDF/Acta_Biomaterialia_BPLP_PLGA_2015.pdf
主要内容:
本研究报道了一系列具备生物可降解性和荧光成像功能的共聚物——生物可降解光致发光聚乳酸-羟基乙酸共聚物(BPLP-co-PLGA),旨在解决传统PLGA需结合细胞毒性量子点或易光漂白有机染料实现荧光标记的缺陷。光致发光表征显示,BPLP-co-PLGA的溶液、薄膜及纳米颗粒均具有强荧光、可调节性及荧光稳定性。通过调整丙交酯(LA)/乙交酯(GA)以及(LA+GA)/BPLP的摩尔比,可使BPLP-co-PLGA在8-16周内完全降解,其荧光衰减行为可用于无创监测材料降解过程。体外细胞毒性和体内异物反应评估表明,BPLP-co-PLGA的生物相容性与常规PLGA相当。研究将该荧光功能化PLGA制成多孔支架(可通过无创成像监测降解)和纳米颗粒,后者通过荧光细胞标记、成像及5-氟尿嘧啶的持续递送,展现出诊疗一体化潜力。该研究为PLGA在荧光需求场景(如组织工程、分子成像、药物递送)的应用拓展提供了新策略。





 齐岳微信公众号
齐岳微信公众号 官方微信
官方微信 库存查询
库存查询