DOTA-NHS是分子影像与核药领域的核心双功能螯合原料,兼具金属离子强螯合能力与蛋白 / 抗体偶联活性,是 PET、SPECT、MRI 等影像探针的关键连接单元,直接决定探针稳定性、标记效率与成像信噪比,为精准诊断与诊疗一体化提供必需的原料支撑。
一、DOTA-NHS原料的基本信息
英文名称:DOTA-NHS ester、DOTA mono-NHS ester
中文名称:1,4,7,10 - 四氮杂环十二烷 - 1,4,7,10 - 四乙酸单 - N - 羟基琥珀酰亚胺酯
CAS 号:170908-81-3,分子式:C₂₀H₃₁N₅O₁₀,分子量:501.49
纯度:≥98%(高纯 / 影像级)结构:DOTA 大环螯合骨架 + NHS 活性酯偶联基团
核心用途:标记抗体、多肽、蛋白,螯合⁶⁸Ga、⁶⁴Cu、¹⁷⁷Lu、Gd 等金属核素 / 离子,用于 PET/MRI 分子影像。
结构式:
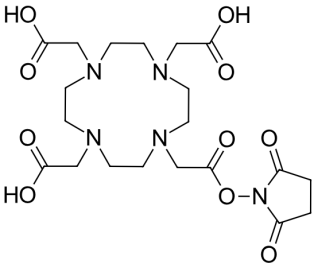
二、DOTA-NHS 的CDMO服务全流程业务
西安齐岳生物拥有专业的CDMO服务团队,可以为客户构建从医药原辅料DOTA-NHS的工艺开发到非GMP公斤级供应的全链条DOTA-NHS服务体系,覆盖工艺开发、中试放大、杂质研究、稳定性研究、质量标准建立、非GMP公斤级供应、GMP申报及GMP供应等核心环节,各环节均建立标准化流程与严格质量管控。

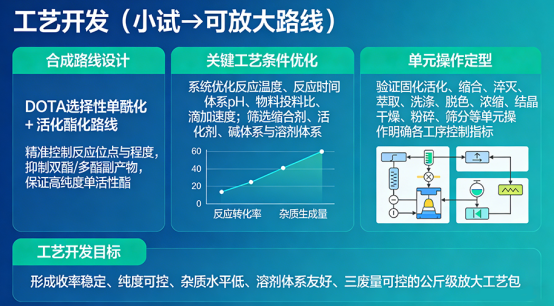
1. 工艺开发(小试→可放大路线)
以影像级原料为目标,开展从实验室小试到可工业化放大的全流程工艺开发。
合成路线设计:采用DOTA 选择性单酰化 + 活化酯化路线,通过精准控制反应位点与反应程度,抑制双酯、多酯等副产物生成,从源头保证产物为高纯度单活性酯,满足偶联标记与核素螯合要求。路线选择优先考虑原子经济性、溶剂安全性、后处理简便性、可放大性。
关键工艺条件优化:系统优化反应温度、反应时间、反应体系 pH、物料投料比、滴加速度等参数;筛选缩合剂、活化剂、碱体系与溶剂体系,在提高反应转化率与选择性的同时,降低杂质生成。通过多组平行试验与正交 / DoE 设计,确定关键工艺参数(CPP)与稳健操作窗口。
单元操作定型:对活化、缩合、淬灭、萃取、洗涤、脱色、浓缩、结晶、干燥、粉碎、筛分等单元操作进行逐一验证与固化,明确各工序控制指标,形成步骤清晰、参数明确、可重复、可放大的标准化操作流程。
工艺开发目标:最终形成收率稳定、纯度可控、杂质水平低、溶剂体系友好、三废量可控的公斤级放大工艺包,为中试及工业化生产提供可靠技术支撑。
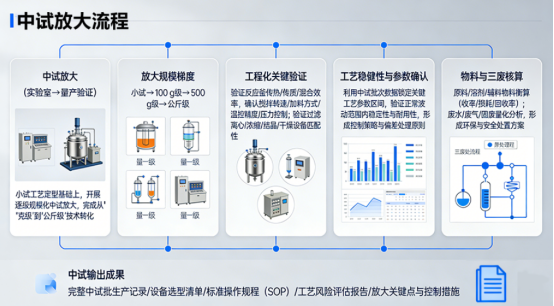
2. 中试放大(实验室→量产验证)
在小试工艺定型基础上,开展逐级规模化中试放大,完成从 “克级” 到 “公斤级” 的技术转化。
放大规模梯度:按照小试 → 100 g 级 → 500 g 级 → 公斤级的路径逐级放大,降低跨量级放大风险,保证工艺平稳过渡。
工程化关键验证:重点验证反应釜传热、传质、混合效率,确认搅拌转速、加料方式、温控精度、压力控制等工程参数;对过滤、离心、浓缩、结晶、干燥等设备的匹配性与适用性进行验证,确保各单元操作在规模化条件下稳定运行。
工艺稳健性与参数确认:利用中试批次数据,进一步锁定关键工艺参数区间,验证工艺在正常波动范围内的稳定性与耐用性,形成可用于生产的控制策略与偏差处理原则。
物料与三废核算:完成原料、溶剂、辅料的物料衡算,统计收率、损耗、回收率;对废水、废气、固废进行量化分析,形成环保与安全处置方案。
中试输出成果:输出完整中试批生产记录、设备选型清单、标准操作规程(SOP)、工艺风险评估报告、放大关键点与控制措施,为后续规模化生产提供完整技术文件。
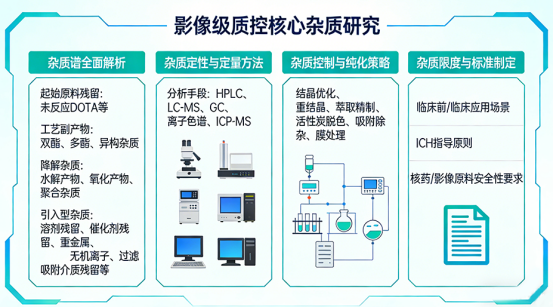
3. 杂质研究(影像级质控核心)
围绕影像探针与核药原料的高安全要求,开展系统、全面的杂质研究与控制。
杂质谱全面解析对工艺全过程可能产生的杂质进行识别与归类:
起始原料残留:未反应 DOTA 等
工艺副产物:双酯、多酯、异构杂质
降解杂质:水解产物、氧化产物、聚合杂质
引入型杂质:溶剂残留、催化剂残留、重金属、无机离子、过滤吸附介质残留等
杂质定性与定量方法:采用 HPLC、LC-MS、GC、离子色谱、ICP-MS 等多种分析手段,完成杂质结构鉴定、来源追溯、定量方法开发,建立专属、灵敏、准确的杂质检测方法,实现对微量杂质的有效监控。
杂质控制与纯化策略:通过结晶优化、重结晶、萃取精制、活性炭脱色、吸附除杂、膜处理等手段,定向降低关键杂质水平;结合工艺条件调整,从反应源头减少杂质生成,实现全过程杂质可控。
杂质限度与标准制定:结合临床前 / 临床应用场景、ICH 指导原则、核药 / 影像原料安全性要求,科学制定杂质控制限度与可接受标准,形成完整杂质控制策略与控制档案。
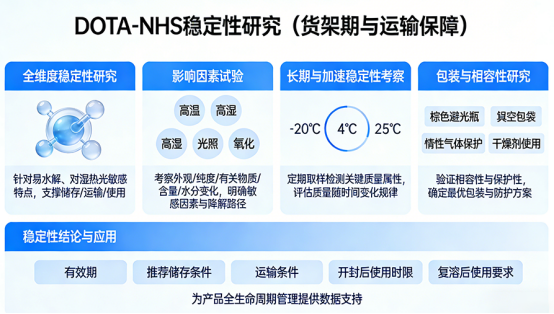
4. 稳定性研究(货架期与运输保障)
针对 DOTA-NHS 易水解、对湿热光敏感的特点,开展全维度稳定性研究,支撑产品储存、运输与使用。
影响因素试验:开展高温、高湿、光照、氧化等强胁迫条件试验,考察产品在极端条件下的外观、纯度、有关物质、含量、水分变化趋势,明确产品敏感因素与降解路径。
长期与加速稳定性:考察在 -20℃、4℃、25℃ 等不同条件下开展长期稳定性与加速稳定性试验,定期取样检测关键质量属性,评估产品质量随时间的变化规律。
包装与相容性研究:对包装材料(棕色避光瓶、铝箔袋、真空包装)、惰性气体保护、干燥剂使用等进行相容性与保护性验证,确定最优包装形式与防护方案。
稳定性结论与应用:依据研究结果,确定产品有效期、推荐储存条件、运输条件、开封后使用时限、复溶后使用要求,为产品全生命周期管理提供数据支持。
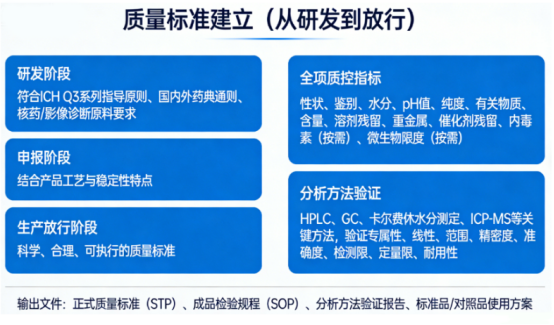
5. 质量标准建立(从研发到放行)
建立符合研发、申报、生产放行全场景需求的质量标准与分析体系。
标准制定:依据遵循 ICH Q3 系列指导原则、国内外药典通则、核药 / 影像诊断原料相关要求,结合产品自身工艺与稳定性特点,建立科学、合理、可执行的质量标准。
全项质控指标覆盖:性状、鉴别、水分、pH 值、纯度、有关物质、含量、溶剂残留、重金属、催化剂残留、内毒素(按需)、微生物限度(按需)等,实现从理化到安全的全方位控制。
分析方法开发与验证:对 HPLC、GC、卡尔费休水分测定、ICP-MS 等关键分析方法进行全面验证,包括专属性、线性、范围、精密度、准确度、检测限、定量限、耐用性等,确保方法可靠、数据可比。
输出文件:形成正式质量标准(STP)、成品检验规程(SOP)、分析方法验证报告、标准品 / 对照品使用方案,支持产品放行、内部质控与外部申报。
6. 非 GMP 公斤级稳定供应
面向临床前研究、早期探针开发、工艺摸索,提供高纯度、批间稳定的非 GMP 规模化供应。
生产与批量:具备百克至公斤级连续批次生产能力,可满足高校、科研院所、药企早期研发的多批次、持续供货需求。
质量保障:执行严格内控质量标准,保证批间一致性、杂质谱稳定、纯度达标,每批次随货提供完整 COA 及关键质检图谱。
包装与交付:采用低温、干燥、避光、密封包装,支持冷链运输;提供常规包装与定制化分装规格,满足不同用量场景。
适用范围:主要用于临床前药效研究、探针标记工艺开发、体外诊断试剂研发、动物实验、方法学建立等非临床用途。

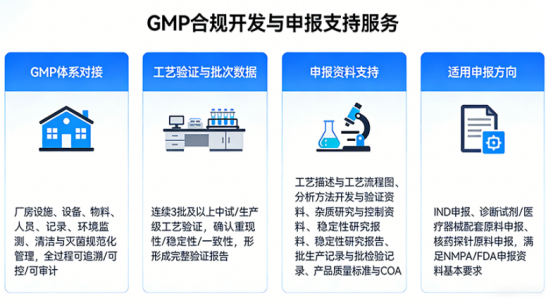
7. GMP 合规开发与申报支持
为进入临床研究与正式申报提供从工艺到合规的全链条 GMP 开发服务。
GMP 体系对接按照 GMP 要求对厂房设施、设备、物料、人员、记录、环境监测、清洁与灭菌等进行规范化管理,保证全过程可追溯、可控、可审计。
工艺验证与批次数据完成连续3 批及以上中试 / 生产级工艺验证,确认工艺在 GMP 条件下的重现性、稳定性与一致性,形成完整验证报告。
申报资料支持可提供全套注册申报支持资料,包括:
工艺描述与工艺流程图
分析方法开发与验证资料
杂质研究与控制资料
稳定性研究报告
批生产记录与批检验记录
产品质量标准与 COA
适用申报方向支持 IND 申报、诊断试剂 / 医疗器械配套原料申报、核药探针原料申报等,满足 NMPA/FDA 申报资料基本要求。
 8. GMP 级商业化供应
8. GMP 级商业化供应
面向临床阶段及商业化项目,提供稳定、合规、可长期合作的 GMP 级原料供应。
GMP 生产条件:在 GMP 受控环境下组织生产,执行偏差管理、变更控制、OOS/OOT 调查、批放行审核体系,全程符合 GMP 规范。
质量放行与追溯:每一批次均按既定质量标准全项检验,经质量部门审核放行,提供完整、可追溯的批生产与检验文件。
供应链与合作模式:具备稳定产能与可靠供应链,支持长期供货协议、定制化包装、质量协议、客户审计等商业化合作模式。
适用场景:用于 I/II/III 期临床阶段影像探针、诊疗一体化药物、NMPA/FDA 申报及商业化生产用关键原料。

三、齐岳生物相关案例分享:
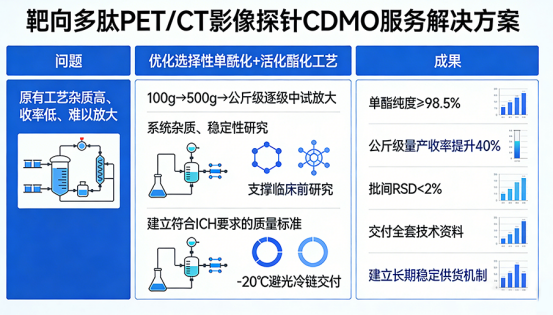
某创新药企研发靶向多肽PET/CT影像探针,需影像级DOTA-NHS原料及从工艺开发到稳定供货的一站式CDMO服务,解决其原有工艺杂质高、收率低、难以放大的问题。
齐岳生物针对性提供解决方案:
优化选择性单酰化+活化酯化工艺,按100g→500g→公斤级逐级中试放大;开展系统杂质、稳定性研究,建立符合ICH要求的质量标准;提供-20℃避光冷链交付,保障批间一致性。
项目成果:交付单酯纯度≥98.5%的影像级DOTA-NHS,公斤级量产收率提升40%,批间RSD<2%,交付全套技术资料,支撑客户完成探针标记、小动物成像等临床前研究,建立长期稳定供货机制。
四:总结订购流程或订购须知
DOTA-NHS 影像类原料CDMO业务订购须知:
确认需求:客户需提供明确的生产规模(克级 / 公斤级 / 百公斤级)、纯度标准(≥99% 可定制)、应用场景及交付节点,同步提供项目合规要求。
前期对接:和客户签保密协议,提供项目详情,工艺放大能力、GMP合规性及年产能,敲定定制化方案与报价后签订正式合同;
质量要求:我们交付随货附 COA,提供 NMR/LC-MS等检测报告,全程监控生产过程,支持定制杂质限度、稳定性研究等需求;
交付验收:协商冷链 / 避光等运输条件、西林瓶 / 铝听等包装形式,到货后按合同标准验收,问题及时对接;
合规支持:我方可协助客户完成 DMF 备案,提供符合 NMPA/FDA 要求的 CMC 申报相关资料,技术资料交付后按协议约定承担保密责任。
售后保障:产品质保期 1 年(按指定条件储存),质保期内非人为原因出现质量问题可退换货;全程提供技术咨询,配合客户解决产品应用相关问题。




 齐岳微信公众号
齐岳微信公众号 官方微信
官方微信 库存查询
库存查询