西安齐岳生物依托成熟的纳米载体制备与细胞膜仿生修饰平台,专注提供细胞膜包裹小分子药物个性化定制服务,覆盖多类细胞膜源、多种小分子药物、全流程技术支撑,可满足较高校科研、药企研发等多场景实验需求。
细胞膜包裹小分子药物是新一代仿生纳米递药技术,通过将天然细胞膜包覆于载药纳米内核表面,赋予纳米药物天然细胞的生物特性,可有效规避机体免疫清除、延长体内循环时间、提升病灶部位靶向富集效率,大幅降低小分子药物的毒副作用,解决传统小分子药物水溶性差、半衰期短、靶向性弱、全身毒性大等临床转化痛点。
一、定制方向
本项定制围绕小分子药物的体内递送痛点,聚焦仿生递药核心需求,从应用场景、药物适配、功能优化三大维度明确定制方向,可根据客户实验目标灵活组合,全方位覆盖小分子药物的科研与转化需求,核心定制方向如下表所示:
定制大类 | 具体定制方向 | 核心研发目标 |
*肿瘤小分子药物递送 | 化疗小分子靶向递药、耐药肿瘤递药、肿瘤微环境响应释药 | 提升肿瘤部位药物富集度,降低化疗药心脏、肝肾毒性,逆转肿瘤多药耐药 |
*炎镇痛小分子药物递送 | 炎症部位靶向递药、长效缓释*炎、降低胃肠道刺激 | 延长药物作用时间,减少给药频次,规避非特异性*炎带来的副作用 |
心脑血管小分子药物递送 | 靶向缺血部位递药、跨越血脑屏障递药、长效稳定释药 | 提升药物病灶局部浓度,改善药物水溶性与生物利用度,实现精准* |
功能优化定制方向 | 长循环优化、主动靶向优化、荧光示踪优化、刺激响应释药优化 | 延长体内半衰期,实现药物实时示踪,实现病灶部位可控释药 |
二、定制类型
根据细胞膜来源、内核载体、药物种类、功能特性划分定制类型,客户可直接按需选择,类型覆盖全面,适配不同实验体系与动物模型,每类定制均可保证粒径均一、包覆率达标、药物包封率稳定,具体定制类型如下:
分类依据 | 具体定制类型 | 适用场景说明 |
细胞膜来源类型 | 红细胞膜、肿瘤细胞膜、巨噬细胞膜、血小板膜、干细胞膜 | 红细胞膜实现长循环;肿瘤细胞膜实现同源靶向;巨噬细胞膜靶向炎症/肿瘤 |
载药内核类型 | 聚合物纳米粒(PLGA/PLA)、介孔二氧化硅纳米粒、脂质体、纳米胶束 | 适配不同溶解性小分子药物,保证较高包封率与缓释性能 |
小分子药物类型 | 化疗药(阿霉素/紫杉醇/顺铂)、*炎药(布洛芬/地塞米松)、心脑血管药 | 覆盖临床常用难溶性小分子药物,可定制单一载药与联合载药 |
功能化定制类型 | 普通仿生载药、荧光标记载药、靶向修饰载药、pH/还原响应载药 | 满足基础递药、活体成像、靶向*、可控释药等不同科研需求 |
三、核心技术支持
齐岳生物拥有完善的细胞膜提取、纳米载药、仿生包覆、质量表征技术平台,全程把控定制工艺,解决细胞膜易破损、包覆率低、药物突释等技术难题,为每一项定制提供硬核技术支撑,核心技术体系如下:
技术板块 | 核心技术内容 | 技术优势 |
细胞膜提取纯化技术 | 低渗裂解-梯度离心法、机械破碎-超滤纯化法 | 保留细胞膜完整性与膜蛋白活性,无蛋白残留,纯度≥95% |
纳米载体制备技术 | 乳化溶剂挥发法、薄膜分散法、静电自组装法、透析法 | 粒径可控(50-200nm),分散性*,药物包封率可达60%-90% |
细胞膜仿生包覆技术 | 挤出式包覆法、超声辅助包覆法、静电吸附包覆法 | 包覆均匀,包覆率≥85%,不破坏细胞膜结构,内核药物无泄漏 |
质量表征检测技术 | TEM电镜表征、DLS粒径检测、Zeta电位检测、包封率/载药量检测 | 提供完整表征数据,可出具检测报告,保证产品质量达标 |
四、案例
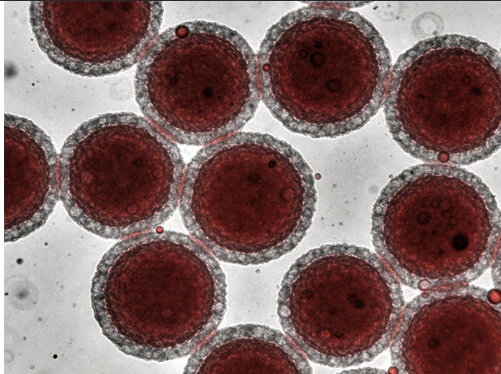
案例:红细胞膜包裹阿霉素PLGA纳米粒定制
定制需求:某较高校医学院定制红细胞膜包裹阿霉素PLGA纳米粒,粒径100±15nm,用于小鼠肿瘤模型靶向化疗,要求长循环、低毒性、肿瘤富集效果好。
定制成果:
五、定制服务流程
全程标准化、透明化服务,周期可控,客户可快速了解全服务环节:
六、可提供相关产品
• 细胞膜包裹化疗小分子药物:红细胞膜包裹紫杉醇纳米粒、肿瘤细胞膜包裹顺铂纳米粒、巨噬细胞膜包裹阿霉素纳米粒
• 细胞膜包裹*炎小分子药物:血小板膜包裹布洛芬纳米粒、干细胞膜包裹地塞米松纳米粒
• 荧光标记细胞膜载药产品:FITC/Cy5/Cy7标记细胞膜包裹小分子药物纳米粒
• 空白细胞膜包覆纳米载体:空白红细胞膜纳米载体、空白肿瘤细胞膜纳米载体(可自行载药)
• 刺激响应型细胞膜载药产品:pH响应细胞膜包裹小分子药物、还原响应细胞膜包裹小分子药物
七、相关文献与文章支持
1. Zhang L, et al. Erythrocyte Membrane-Coated Nanoparticles for Long-Circulating Chemotherapeutic Drug Delivery. Advanced Materials, 2021, 33(45): 2103456.
2. Wang Y, et al. Cancer Cell Membrane-Coated Biomimetic Nanocarriers for Homologous Targeted Tumor Therapy. Biomaterials, 2022, 280: 121389.
3. Liu H, et al. Macrophage Membrane-Coated Nanoparticles for Inflammation-Targeted Delivery of Small-Molecule Anti-Inflammatory Drugs. Journal of Controlled Release, 2023, 354: 114782.
4. Zhao Q, et al. Cell Membrane-Coated Bionic Nanomedicine: A Promising Platform for Small Molecule Drug Delivery. Advanced Drug Delivery Reviews, 2024, 198: 114896.
5. Chen X, et al. Platelet Membrane-Coated Nanoparticles for Targeted Treatment of Cardiovascular Diseases. Nano Letters, 2022, 22(8): 3210-3218




 齐岳微信公众号
齐岳微信公众号 官方微信
官方微信 库存查询
库存查询