靶向脂质体作为一种可调控的纳米递送载体,通过表面配体修饰可实现对目标细胞的选择性识别。其中,叶酸(FA)及 RGD 肽修饰已被广泛应用于受体介导的递送研究中,可用于提升分子递送的选择性与过程可控性。
针对不同研究需求,西安齐岳生物提供靶向脂质体定制服务,涵盖FA、RGD肽等配体修饰体系,支持PEG修饰、荧光标记及多种分子包封设计。同时提供从脂质体构建到基础表征的一体化服务,适用于多种实验与研究场景。
一、核心定制产品(叶酸/RGD修饰靶向脂质体)
依托成熟技术,可定制不同规格的叶酸/RGD修饰靶向脂质体,涵盖科研级、药物研发级、临床前级,支持单修饰、双修饰定制,核心参数可按需调整:
1. 叶酸(FA)修饰靶向脂质体
• 核心修饰:叶酸通过PEG链偶联至脂质体表面,常用载体DSPE-PEG2000-FA,保障靶向性与长循环,避免被网状内皮系统快速吞噬。
• 靶向机制:与肿瘤细胞(乳腺癌、宫颈癌等)表面高表达的叶酸受体特异性结合,介导胞吞递药,适用于叶酸受体阳性肿瘤的治疗与成像研究。
• 可定制参数:粒径50-300nm(常用100-150nm)、PDI≤0.2、包封率≥80%(小分子)/≥90%(核酸)、叶酸偶联率≥90%,批次差异<5%。
• 适配负载物:小分子化疗药、核酸、荧光探针、蛋白/多肽,可结合pH、还原响应等智能释药功能定制。
• 储存条件:-20℃冷冻干燥保存,避免频繁冻融,保质期6-12个月(依负载药物调整)。
2. RGD肽修饰靶向脂质体
• 核心修饰:RGD肽通过酰胺键或无铜点击化学偶联,常用载体DSPE-Hyd-PEG-RGD,可搭配pH响应腙键实现肿瘤微环境响应释药。
• 靶向机制:特异性结合肿瘤细胞及新生血管内皮细胞表面的整合素αvβ3、αvβ5,适用于黑色素瘤、胶质瘤等整合素高表达肿瘤的靶向递送。
• 可定制参数:粒径50-200nm(精准调控)、PDI≤0.18、包封率≥85%、RGD偶联率≥88%,支持cRGD、iRGD等衍生物修饰。
• 适配负载物:化疗药、光热剂、基因药物、造影剂,可结合穿膜肽提升胞内释药效率,适配协同治疗、基因治疗等场景。
• 储存条件:-20℃冷冻干燥保存,密封避光,可定制冻干保护剂延长储存周期。
3. 叶酸+RGD双修饰靶向脂质体
结合两种靶向优势实现双重靶向,提升肿瘤富集效率、降低脱靶效应,可定制叶酸与RGD修饰比例(1:1至3:1),适用于复杂肿瘤微环境下的精准递送。
二、定制案例分享
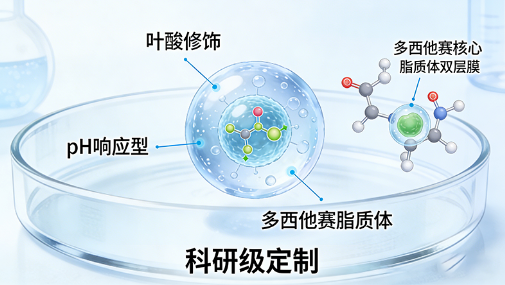
案例1:叶酸修饰pH响应型多西他赛脂质体(科研级定制)
• 客户需求:高校肿瘤学课题组需定制叶酸修饰pH响应脂质体,负载多西他赛,用于黑色素瘤药效研究,要求粒径150nm左右、包封率≥85%,具备酸性响应释药能力。
• 定制方案:采用薄膜水化-挤出法,选用DSPE-PEG2000-FA等脂质组分,引入pH敏感腙键与DiD荧光探针,通过硫酸铵梯度法提升包封率,优化叶酸偶联工艺。
案例2:RGD修饰siRNA脂质体(药物研发级定制)
• 客户需求:生物医药企业需定制RGD修饰阳离子脂质体,负载survivin基因siRNA,用于卵巢癌研发,要求粒径80-100nm、转染效率≥80%,无明显毒性、批次稳定。
• 定制方案:微流控法制备,选用DOTAP、DSPE-PEG2000-RGD等组分,电荷复合包封siRNA,优化脂质与siRNA比例,保障RGD活性与siRNA完整性。

三、定制服务流程
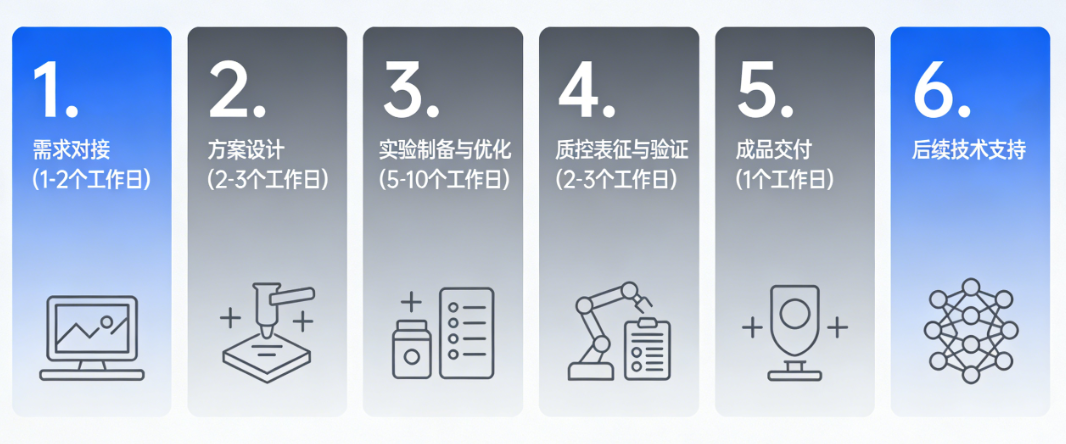
1. 需求对接(1-2个工作日):客户提供修饰类型、负载物、参数、用途等需求,技术团队一对一沟通确认,解答疑问。
2. 方案设计(2-3个工作日):制定个性化方案,明确脂质组分、制备工艺、质控标准,客户确认后启动制备。
3. 实验制备与优化(5-10个工作日):选用高纯度原料(磷脂≥98%),优化关键参数,及时反馈进度与数据。
4. 质控表征与验证(2-3个工作日):全面检测粒径、包封率等指标,提供完整质控报告。
5. 成品交付(1个工作日):冷冻干燥成品配说明书、质控报告发货,提供使用指导。
6. 后续技术支持:售后咨询,可优化方案助力实验开展。
四、核心优势
• 技术成熟:多年定制经验,熟练掌握单/双修饰技术,可解决智能响应、大规模制备等难题。
• 质控严格:高纯度原料,标准化流程,每批全面质控,保障批次稳定,满足科研与研发严谨性要求。
• 灵活定制:支持毫升级至克级定制,可灵活调整参数,适配不同实验场景。
• 全程服务:一对一对接,从方案到售后全程跟进,提供专业指导,降低研发成本。
五、参考文献
1. Gabizon A, Papahadjopoulos D. Stealth liposomes: a review(J). Cancer Research, 1988, 48(18): 5146-5152.(PEG化长循环脂质体奠基文献)
2. Immordino ML, Dosio F, Cattel L. Pegylation of liposomes for anticancer drug delivery(J). Int J Pharm, 2006, 316(1-2): 1-20.(叶酸靶向磷脂肿瘤富集验证)
3. Wang Y, Li X, Zhang L. Structure-guided design of pH-responsive phospholipids(J). Adv Healthcare Mater, 2022, 11(12): 2200456.(智能响应脂质体设计参考)
4. RGD peptide-modified pH-sensitive liposomes enhance doxorubicin's effect on breast cancer(J). J Biomed Mater Res A, 2020, https://doi.org/10.1007/s11095-020-02968-5.(RGD靶向效果验证)
5. Li C, et al. Berberine-inspired ionizable lipid for nucleic acid delivery. Nat Commun, 2025, 16(1): 1287.(脂质体稳定性优化技术)
6. Wang H#, Ding T#, Guan J, et al. Interrogation of folate-functionalized nanomedicines. ACS Nano, 2020, 14(11): 14779-14789.(叶酸修饰递送机制研究)
7. 整合素受体介导共载双药脂质体的构建及*肿瘤研究[J]. 中国生物医学文献服务系统, 2025.(RGD双药负载研究)
8. pH-sensitive hydrazone-linked DSPE-PEG liposomes for tumor delivery(J). J Control Release, 2018, https://doi.org/10.1016/j.jconrel.2018.05.021.(pH敏感修饰技术)
可根据实验方向补充参考文献,如需了解原料、周期、报价等细节,可对接技术团队获取个性化方案。




 齐岳微信公众号
齐岳微信公众号 官方微信
官方微信 库存查询
库存查询