西安齐岳生物专注于脂质体研发外包CDMO服务,依托专业的技术团队、完善的实验平台及丰富的项目经验,为客户提供从原辅料筛选到非GMP公斤级供应的全流程、一体化脂质体研发外包服务,覆盖脂质体研发、工艺、验证、生产全链条,精准满足客户从实验室小试到中试放大的各类需求,助力客户加速脂质体相关产品的研发进程。
一、核心服务概述
西安齐岳生物脂质体研发外包CDMO业务全面覆盖脂质体研发全生命周期,具体包含:脂质体原辅料筛选、配方开发、配方脂质体系统验证与生物学评价、脂质体配方的工艺开发及中试放大、分析方法开发及验证、稳定性研究和质量标准建立、脂质体质量标准建立、非GMP公斤级供应等核心服务,可根据客户需求提供定制化解决方案,全程保障服务的专业性、合规性与高效性。

二、详细服务内容
1. 脂质体原辅料筛选
围绕脂质体产品研发的核心需求,筛选适配性强、质量可控、可追溯的原辅料,为后续配方开发和工艺优化奠定基础,全程遵循药用级标准,保障原辅料的安全性与合规性。
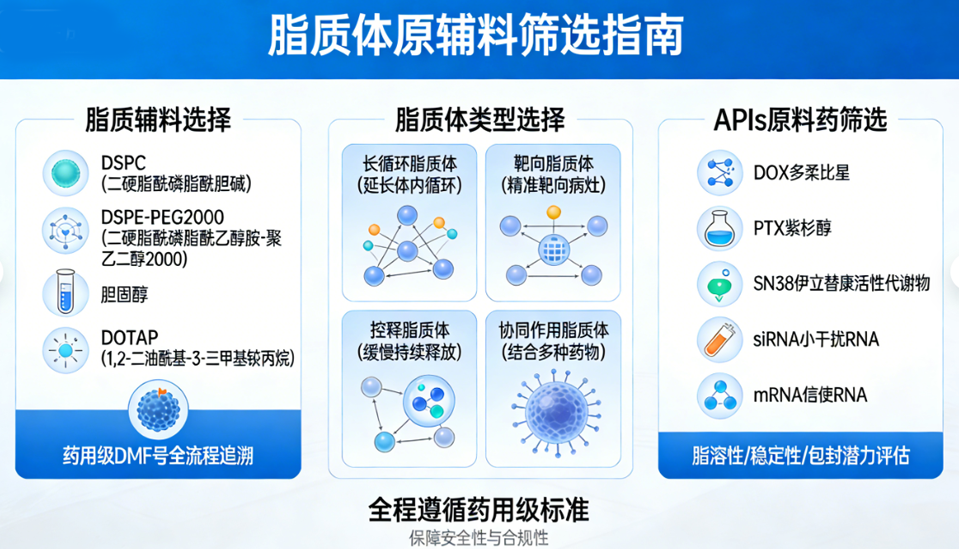
(1)脂质辅料选择:精选药用级脂质辅料,涵盖DSPC(二硬脂酰磷脂酰胆碱)、DSPE-PEG2000(二硬脂酰磷脂酰乙醇胺-聚乙二醇2000)、胆固醇、DOTAP(1,2-二油酰基-3-三甲基铵丙烷)等常用品类,所有脂质辅料均提供正规药用DMF号,可实现全流程追溯,确保辅料质量符合药用标准,适配不同脂质体产品的研发需求。
(2)脂质体类型选择:根据客户产品定位、药物特性及临床需求,提供个性化脂质体类型选择建议,可定制长循环脂质体(延长体内循环时间,减少网状内皮系统清除)、靶向脂质体(精准靶向病灶部位,提高局部药物浓度,降低全身毒副作用)、控释脂质体(实现药物缓慢、持续释放,延长药效时长)或协同作用脂质体(结合多种药物或载体,提升治疗效果)。
(3)APIs原料药筛选:针对脂质体包封需求,筛选适配的原料药,包括脂质体包封化小分子药物(如DOX多柔比星、PTX紫杉醇、SN38伊立替康活性代谢物等常用抗肿瘤药物)、核酸类药物(siRNA小干扰RNA、mRNA信使RNA等),重点评估原料药的脂溶性、稳定性、包封潜力,确保原料药可高效包封于脂质体中,且包封后能保持其生物活性。
2. 配方开发
以“高包封率、优稳定性、适配工艺”为核心目标,开展全流程配方开发工作,从初步摸索到优化定稿,提供完整的配方方案及小试样品,满足后续研发及验证需求。
(1)脂质体配方开发:结合原辅料筛选结果,系统优化脂质与药物的配比比例,重点调控包封效率(目标包封率根据药物类型可达80%以上,部分小分子药物可突破90%)、粒径大小(常规调控在50-200nm,可根据靶向需求调整粒径范围),设计符合稳定性要求的处方,兼顾脂质体的分散性与均一性。
(2)初步工艺摸索:针对不同药物特性,筛选适配的脂质体制备工艺,主要包括薄膜法(适用于脂溶性药物,操作简便、 reproducibility好)、乙醇注入法(适用于水溶性药物,包封效率高、粒径均匀)、微流控法(可实现精准控温、控速,制备的脂质体粒径均一性佳,适配规模化生产),初步确定各工艺的关键操作参数。
(3)配方指标优化:对脂质体核心指标进行系统性优化,包括粒径(控制PDI≤0.3,确保脂质体分散均匀)、Zeta电位(根据脂质体类型调控电位范围,通常为-20~+30mV,提升脂质体稳定性)、包封率(优化至最优水平,减少药物泄漏)、药物释放曲线(根据临床需求,调控药物释放速率,实现速释或缓释效果)、稳定性(确保配方在短期储存条件下无明显降解、聚集)。
(4)处方稳定性研究:开展短期稳定性研究(为期2–4周),模拟常规储存条件(2-8℃、室温),监测脂质体粒径、包封率、外观等指标变化;同时进行冻融稳定性测试(反复冻融3-5次)、光照/温度影响测试(强光照射、高温加速条件),评估处方在极端条件下的稳定性,排除不稳定因素。
(5)冻干处方开发:针对需要长期储存的脂质体产品,开展冻干处方开发,筛选适配的冻干保护剂(如甘露醇、蔗糖、海藻糖等),优化保护剂与脂质体的配比比例,重点考察冻干后产品的复溶性(复溶时间≤5分钟)、粒径恢复率(恢复率≥95%),确保冻干后脂质体的结构完整性与生物活性。
(6)处方优化和小试样品供应:基于上述研究,对处方进行最终优化,确定最优配方方案,同时提供足量小试样品(通常为10-100mL,可根据客户需求调整),附带完整的小试数据报告,包括配方参数、指标检测结果、稳定性数据等,为客户后续实验提供支撑。
3. 配方脂质体系统验证与生物学评价(生物学&体内体外)
通过体内、体外实验及影像追踪,全面验证脂质体配方的生物相容性、有效性及靶向性,为配方优化和产品研发提供科学依据,全程遵循标准化实验流程,确保实验数据的真实性、可靠性。
(1)体外实验:开展细胞水平验证,包括细胞摄取率测试(采用荧光标记法,检测细胞对脂质体的摄取效率,目标摄取率根据细胞类型可达60%以上)、转染效率测试(针对核酸类脂质体,检测mRNA/siRNA的转染效果,转染效率≥80%)、细胞毒性测试(采用CCK-8法,评估脂质体对正常细胞的毒性,确保安全剂量范围),同时可根据客户需求开展体外药物释放实验,模拟体内生理环境,检测药物释放规律。
(2)体内实验:依托小动物实验平台,开展体内药效学(PD)、药代动力学(PK)、生物分布及毒理学研究。药代动力学研究(PK):检测脂质体在小鼠、大鼠等小动物体内的吸收、分布、代谢、排泄规律,计算半衰期、血药浓度-时间曲线下面积(AUC)等关键参数;药效学研究(PD):建立相应疾病模型(如肿瘤模型、炎症模型),评估脂质体产品的治疗效果,对比空白脂质体与载药脂质体的药效差异;生物分布研究:检测脂质体在体内各器官(心、肝、脾、肺、肾及病灶部位)的分布情况,验证靶向脂质体的靶向效率;毒理学研究:评估脂质体的急性毒性、亚急性毒性,检测体重变化、器官指数、血常规、肝肾功能等指标,确保脂质体的安全性。
(3)影像追踪:利用客户提供的荧光探针或标记分子,对脂质体进行标记,通过小动物活体成像技术,实时追踪脂质体在体内的分布情况、靶向部位及代谢过程,直观呈现脂质体的体内行为,为配方优化和靶向性验证提供可视化数据支撑。
4. 脂质体配方的工艺开发及中试放大
基于小试配方及工艺,开展工艺优化与中试放大,解决工艺规模化过程中的技术难题,确保放大后产品质量与小试产品一致,为后续工业化生产奠定基础,全程注重工艺的稳定性、可重复性与合规性。
(1)工艺路线选择:结合药物的理化性质(脂溶性、水溶性、稳定性)、生产规模需求及客户预算,选择最优的脂质体制备工艺路线,对薄膜法、乙醇注入法、微流控法等工艺进行对比验证,确定适配规模化生产、且能保障产品质量的工艺路线,同时提供工艺路线选择的依据及对比数据。
(2)工艺参数优化:对选定的工艺路线进行关键参数优化,包括高压均质的压力(通常为500-2000bar)、均质次数,溶剂注入速率(根据工艺类型调控为0.1-10mL/min),剪切速率(10000-30000rpm),反应温度(25-60℃),搅拌速度等,通过单因素实验、正交实验等方法,确定最优工艺参数,确保脂质体的粒径、包封率等核心指标稳定达标。
(3)无菌工艺与纯化:针对脂质体制剂的无菌要求,建立完善的无菌工艺,包括原料无菌处理、设备无菌消毒、操作环境无菌控制(符合GMP洁净级别要求),对脂质体制剂进行无菌过滤(采用0.22μm滤膜);同时开展溶剂去除工艺优化,严格控制有机溶剂(如乙醇、氯仿)残留量,确保残留量符合药用标准(通常≤0.1%),避免有害溶剂对产品质量及安全性造成影响。
(4)放大与中试:开展规模放大实验,实现从小试(毫升级)到中试(升级)的平稳过渡,重点验证放大过程的等效性,确认放大后脂质体的粒径、PDI、包封率、Zeta电位等核心指标与小试样品一致;同时评估放大后脂质体的稳定性、均一性,检测工艺的可重复性(连续3批中试产品质量偏差≤5%),确保中试产品质量满足后续研发及生产需求,提供完整的中试报告,包括工艺参数、质量检测数据、放大验证结果等。
5. 分析方法开发及验证
建立科学、精准、可重复的脂质体分析方法,对脂质体的核心质量指标进行检测,同时完成方法学验证,确保分析方法的可靠性与合规性,为产品质量控制提供技术支撑。
(1)粒径与PDI测定:采用动态光散射法(DLS),选择合适的检测条件(温度25℃、检测角度90°),建立粒径与PDI的测定方法,验证方法的精密度(RSD≤5%)、准确性,确保能精准检测脂质体的粒径大小及分散均匀性,检测范围覆盖50-1000nm。
(2)包封率分析:建立包封率的检测方法,通常采用高效液相色谱法(HPLC)或液相色谱-质谱联用法(LC-MS),通过离心、透析等方法分离未包封药物与总药物,检测两者的含量,计算包封率;对方法进行验证,包括精密度、准确度、回收率(回收率在85%-115%之间),确保检测结果准确可靠,适配不同类型药物的包封率检测需求。
(3)表面电位:通过Zeta电位测定仪,建立脂质体表面电位的测定方法,优化检测条件(温度25℃、缓冲液pH值适配脂质体特性),验证方法的精密度,确保能准确反映脂质体的表面电荷情况,为脂质体稳定性评估提供依据。
(4)稳定性监测:建立脂质体稳定性的长期监测方法,定期检测脂质体的粒径变化、PDI、包封率、药物含量、外观等参数,设定监测周期(1个月、3个月、6个月、12个月),评估脂质体的长期稳定性;同时建立加速稳定性、冻融稳定性的检测方法,快速评估脂质体在极端条件下的稳定性变化,为产品储存条件设定提供依据。
6. 稳定性研究和质量标准建立
全面开展脂质体稳定性研究,系统考察不同储存条件对脂质体质量的影响,结合稳定性数据,建立科学、合理的脂质体质量标准,确保产品在保质期内质量稳定、安全有效。
(1)短期稳定性研究:主要评估脂质体在常规储存条件下(2-8℃、室温)一段时间内(2-4周)的质量变化,考察指标包括:粒径(变化幅度≤10%)、包封率(下降幅度≤5%)、外观(无浑浊、分层、沉淀)、PH值(波动范围±0.5)、粒子强度(无明显破损),确保脂质体在短期储存及运输过程中质量稳定。
(2)长期稳定性研究:通过模拟脂质体产品的长期储存条件(2-8℃避光保存),开展为期12-24个月的长期稳定性监测,考察指标包括:温度、湿度、光照对脂质体质量的影响,以及粒径、PDI、包封率、药物释放情况(释放曲线无明显偏移)、外观变化(无浑浊、分层、沉淀)、沉淀物(无明显沉淀生成)、澄清物(保持澄清透明)、药物析出分析(无药物结晶析出),通过长期数据预测脂质体的实际保存期限,为产品保质期设定提供科学依据。
(3)加速稳定性研究:在更高温度(40℃±2℃)和湿度(75%±5%)条件下,开展6个月的加速稳定性研究,观察脂质体的粒径变化、包封率变化(下降幅度≤10%)、药物降解情况(降解率≤5%),通过加速实验数据快速评估脂质体的稳定性,缩短研发周期,同时验证长期稳定性研究的合理性。
(4)冻融稳定性研究:模拟脂质体冻融储存及运输过程,进行反复冻融(-20℃冷冻、25℃解冻,重复3-5次),观察冻融后脂质体的粒径恢复情况(恢复率≥95%)、包封率恢复情况(恢复率≥90%),是否出现分层、沉淀、浑浊等不良现象,优化脂质体配方及冻融条件,确保脂质体在冻融过程中质量稳定。
(5)冻干稳定性研究:针对冻干脂质体产品,开展冻干稳定性研究,考察冻干过程对脂质体结构及质量的影响,包括:重构后粒径的恢复(恢复率≥95%)、包封率和药物活性(包封率下降≤5%,药物活性保留≥90%)、稳定性(冻干后产品在2-8℃储存6个月,质量无明显变化),优化冻干工艺参数,确保冻干脂质体的质量稳定性及复溶性。
7. 脂质体质量标准建立
结合稳定性研究数据、分析方法验证结果及行业标准,建立全面、严格的脂质体质量标准,涵盖产品外观、理化性质、生物学特性等各个方面,确保产品质量可控、安全有效,同时适配后续研发及申报需求。
(1)外观与物理性质:明确脂质体的外观要求(如乳白色混悬液、澄清透明溶液等),设定粒径范围(50-200nm)、PDI限值(≤0.3)、Zeta电位范围(-20~+30mV)、PH值范围(6.0-8.0),确保脂质体的物理性质稳定、均一。
(2)包封率与药物含量:设定包封率限值(根据药物类型≥80%或90%),明确药物含量的限度范围(±5%),确保脂质体的载药效率及药物含量可控,避免药物泄漏或含量不达标。
(3)药物释放特性:根据临床需求,设定药物释放曲线的限度要求,明确不同时间点的药物释放量(如24小时释放量≥80%),确保脂质体的药物释放符合设计要求,实现预期的治疗效果。
(4)稳定性数据:结合长期、加速、短期稳定性研究结果,设定脂质体的保质期(如12个月、24个月),明确储存条件(如2-8℃避光、密封保存),确保产品在保质期内质量稳定。
(5)无菌性与内毒素:针对无菌制剂要求,设定无菌性标准(符合《中国药典》无菌检查法要求),内毒素限值(≤0.5EU/mL),确保脂质体产品无细菌污染、内毒素含量达标,保障使用安全。
(6)生物相容性与生物活性:设定生物相容性标准(如细胞毒性≤2级、无溶血反应),明确药物生物活性的限度要求(如体外细胞抑制率≥80%),确保脂质体产品具有良好的生物相容性及生物活性,满足临床使用需求。
8. 非GMP公斤级供应
依托中试生产平台,为客户提供非GMP级别的公斤级脂质体供应服务,全程遵循标准化生产流程,严格控制产品质量,满足客户用于临床前研究、小批量验证、科研实验等场景的需求。
我们可根据客户的配方要求及用量需求,提供公斤级(1-10kg)脂质体产品,产品质量严格遵循前期建立的质量标准,确保粒径、包封率、稳定性等核心指标达标;同时提供完整的产品质量报告,包括生产工艺参数、质量检测数据、稳定性数据等,全程保障产品的一致性与可靠性;可根据客户需求,提供定制化的包装(如密封西林瓶、输液袋)及储存建议,确保产品在运输及储存过程中质量稳定。
订购流程:





 齐岳微信公众号
齐岳微信公众号 官方微信
官方微信 库存查询
库存查询