西安齐岳生物深耕生物材料定制领域,专注水凝胶材料全链条研发与定制服务,依托专业研发团队、完善的制备平台及严格的质控体系,可根据客户科研、临床前及产业化需求,提供多类型体系水凝胶定制解决方案,涵盖原料改性、凝胶成型、功能化修饰到载药、质控、中试放大的一站式服务,助力客户实现成果转化与技术落地,适配组织工程、药物递送、医美、3D细胞培养、创面修复等多领域应用场景。

一、水凝胶材料按需定制核心内容
齐岳生物水凝胶定制并非单一结构调整,而是基于客户具体需求,从原料、结构、性能、功能、应用场景五大核心维度精准定制,各方向可自由组合搭配,满足个性化科研及应用需求,细分方向如下:
(一)按材料体系定制
• 天然高分子水凝胶:以透明质酸(HA)、明胶、海藻酸盐、壳聚糖、胶原蛋白等为原料,定制具有良好生物相容性、可降解性的水凝胶,适配生物医学领域的细胞培养、组织修复等场景,可根据需求调控降解速率、溶胀度及力学性能,例如透明质酸水凝胶可用于医美填充、创面修复,壳聚糖水凝胶可用于药物递送载体。
• 合成高分子水凝胶:定制聚乙二醇(PEG)、聚乙烯醇(PVA)、聚乳酸-羟基乙酸共聚物(PLGA)、甲基丙烯酰化明胶(GelMA)、聚N-异丙基丙烯酰胺(PNIPAM)等合成材料水凝胶,具有理化性质稳定、力学强度可调、结构可控等优势,可适配柔性可穿戴器件、生物传感器、工业水处理等场景,例如PNIPAM温敏水凝胶可实现温度触发的原位成型与药物释放,GelMA水凝胶可用于3D细胞支架制备。
• 复合水凝胶:结合天然与合成材料的优势,定制壳聚糖-明胶、PEG-PLGA、透明质酸-PEG等复合体系水凝胶,兼顾生物相容性与结构稳定性;同时可定制纳米复合水凝胶,嵌入MXene、ZIF-8等纳米材料,实现功能增强,适配高端科研及特种应用场景,例如负载ZIF-8的复合水凝胶可用于酶类药物的保护与可控释放。
(二)按功能特性定制
• 刺激响应型水凝胶:按需定制pH响应、温度响应、光响应、酶响应、磁场响应等智能水凝胶,可实现特定条件下的凝胶化、溶胀或药物释放,适配精准给药、智能传感等场景。例如pH响应型BSA-GMA水凝胶可用于肿瘤微环境靶向给药,温度响应型水凝胶可实现可注射原位成型,光响应型水凝胶可通过光照调控药物释放速率。
• 载药/载生物活性物质水凝胶:定制可负载小分子药物、蛋白、核酸、酶类、外泌体等生物活性物质的水凝胶,通过物理嵌入、化学结合、纳米粒子复合负载等方式,确保活性物质的稳定性与可控释放,适配药物递送、组织修复等场景,例如负载ZIF-8@chABC的水凝胶微针可用于神经修复,负载*炎药的透明质酸纳米水凝胶可用于皮肤给药缓释。
• 功能性修饰水凝胶:提供表面功能化定制,包括靶向配体修饰、PEG化修饰、荧光标记、磁性修饰等,提升水凝胶的靶向性、生物相容性或可检测性,例如PEG化修饰可延长水凝胶在体内的循环时间,荧光标记水凝胶可用于生物成像与追踪,靶向配体修饰可实现病灶部位精准递送。
(三)按应用场景定制
• 科研实验用水凝胶:适配高校、科研院所的课题研究,定制3D细胞培养支架、生物传感器基材、实验用功能水凝胶,可精准调控孔隙率、力学强度、响应特性等参数,满足实验检测与研究需求,例如飞秒激光直写制备的BSA-GMA 3D水凝胶支架,可用于软骨细胞培养研究。
• 生物医学用水凝胶:定制创面修复水凝胶、组织工程支架水凝胶、药物递送载体水凝胶、水凝胶微针等,注重生物相容性、可降解性及临床适配性,例如负载生长因子的创面修复水凝胶可加速皮肤愈合,软骨修复用复合水凝胶可促进软骨细胞增殖分化。
• 工业及其他领域水凝胶:定制水处理用吸附水凝胶、柔性电子用导电水凝胶、食品保鲜用水凝胶等,根据工业应用需求调控吸附容量、导电性能、机械稳定性等参数,适配不同工业场景的个性化需求。
(四)按结构形态定制
• 宏观水凝胶:定制块状、膜状、凝胶珠等形态,适配组织工程支架、创面敷料、药物缓释植入物等场景,可调控尺寸、厚度及力学性能,例如块状水凝胶支架可用于骨组织修复,膜状水凝胶可用于皮肤创面覆盖。
• 微观水凝胶:定制微球(1–100 μm)、纳米水凝胶(50–500 nm),适配药物递送、细胞载体等场景,可精准调控粒径与分散性,例如50 μm壳聚糖微球可用于蛋白药物长效递送,200 nm GelMA纳米水凝胶可用于肿瘤靶向给药。
• 特殊形态水凝胶:定制可注射水凝胶、水凝胶微针、3D打印水凝胶等,适配微创给药、精准修复、个性化支架制备等场景,例如可注射温敏水凝胶可实现原位成型,水凝胶微针可实现皮肤微创给药,3D打印水凝胶可定制个性化组织工程支架。
二、具体产品展示
齐岳生物依托定制技术,推出多款标准化+定制化水凝胶产品,覆盖多体系、多场景,可根据客户需求进一步优化参数,核心产品如下:
(一)标准化水凝胶产品
产品名称 | 材料体系 | 核心特性 | 适用场景 |
透明质酸水凝胶 | 天然高分子(HA) | 高生物相容性、可降解、高溶胀度,支持功能化修饰 | 医美填充、创面修复、3D细胞培养 |
GelMA水凝胶 | 合成高分子(甲基丙烯酰化明胶) | 光交联、力学强度可调、细胞相容性好 | 3D细胞支架、组织工程、生物打印 |
PNIPAM温敏水凝胶 | 合成高分子(聚N-异丙基丙烯酰胺) | 温度响应(LCST可调)、可注射、原位成型 | 微创给药、原位组织修复 |
负载ZIF-8@chABC水凝胶微针 | 复合体系(HA/PVA+ZIF-8) | 酶活性保护、可控释放、皮肤穿透性好 | 神经修复、软骨退行性病变辅助* |
壳聚糖纳米水凝胶 | 天然高分子(壳聚糖) | 粒径可控(50-500nm)、载药能力强 | 药物递送、靶向* |
(二)定制化产品服务
针对客户特殊需求,提供全流程定制产品开发,包括但不限于:
• 定制特定响应类型(pH/光/酶响应)的智能水凝胶,调控响应阈值与响应速度;
• 定制复合水凝胶体系,嵌入纳米材料、生物活性物质,实现多功能集成;
• 定制特殊形态水凝胶(如定制粒径的微球、个性化3D打印支架、靶向修饰水凝胶);
• 定制工业用功能水凝胶,调控吸附容量、导电性能、机械稳定性等参数。
三、案例分享
齐岳生物已为多家高校、科研院所及企业提供水凝胶定制服务,积累了丰富的案例经验,以下为典型案例展示,保护客户隐私,部分参数已做脱敏处理:
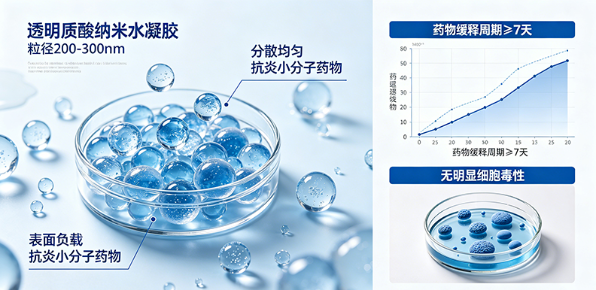
案例1:透明质酸纳米水凝胶载药定制(科研用途)
客户需求:某高校实验室需定制一款负载*炎小分子药物的透明质酸纳米水凝胶,要求粒径200-300nm,分散性好,药物缓释周期≥7天,无明显细胞毒性,用于皮肤给药相关课题研究。
定制方案:选用高纯度透明质酸为原料,采用乳化交联法制备纳米水凝胶,优化交联剂用量与反应条件,调控粒径分布;采用物理嵌入法负载*炎药物,优化负载比例,确保药物包封效率≥85%;通过调整交联度,实现药物缓释周期达9天,满足客户课题需求。
案例2:3D细胞培养支架水凝胶定制(临床前研究)
客户需求:某生物企业需定制一款用于软骨细胞培养的3D支架水凝胶,要求孔隙率80%-85%,力学强度适中(弹性模量10-20kPa),细胞相容性*,可支持软骨细胞增殖分化,适配临床前组织工程研究。
定制方案:采用GelMA与透明质酸复合体系,通过冷冻干燥法制备多孔水凝胶支架,优化制备工艺,调控孔隙结构与力学性能;对支架表面进行改性处理,提升细胞黏附能力;同步提供细胞相容性检测(CCK-8法),确保支架无细胞毒性,可支持软骨细胞高效增殖分化。

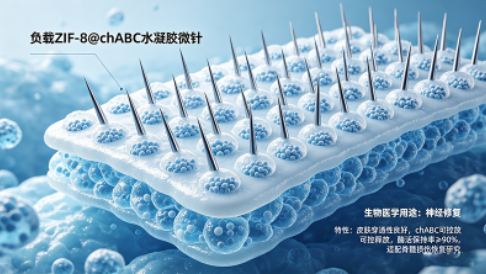
案例3:负载ZIF-8@chABC水凝胶微针定制(生物医学用途)
客户需求:某科研机构需定制一款用于神经修复的水凝胶微针,要求微针具有良好的皮肤穿透性,可负载ZIF-8@chABC纳米复合物,实现chABC的可控释放,酶活保持率≥90%,适配脊髓损伤恢复研究。
定制方案:以透明质酸为微针主体材料,采用微模成型工艺制备水凝胶微针;通过原位包载技术,将ZIF-8@chABC纳米复合物均匀分散于微针中,优化包载比例与制备工艺,确保酶活保持率;检测微针穿刺力与体外释放曲线,实现ZIF-8在微酸性环境下降解释放chABC,满足神经修复研究需求。
四、服务流程
齐岳生物简化服务流程,聚焦定制核心环节,高效响应客户需求,流程如下:
1. 需求沟通:客户提出定制需求(材料体系、功能特性、应用场景、参数要求等),我方专业工程师一对一对接,明确需求细节,提供初步定制方案建议;
2. 方案确认:根据客户需求,出具详细定制方案(含材料选择、制备工艺、性能参数、交付周期、费用明细),与客户沟通确认,修改优化至满意;
3. 样品制备:按照确认方案,开展实验室小试制备,严格控制制备过程,确保样品符合参数要求;
4. 性能检测与交付:对样品进行全面性能检测,出具检测报告,将样品、检测报告及相关技术资料一并交付客户;
5. 售后支持:提供后续技术咨询、样品优化调整服务,协助客户解决使用过程中的相关问题,长期跟进客户需求。
五、参考文献
齐岳生物水凝胶定制技术依托前沿科研成果,参考国内外核心文献,部分相关参考文献如下:
1. Drury, J.L., Mooney, D.J., “Hydrogels for tissue engineering: scaffold design variables and applications”, Biomaterials, 2003.
2. Caló, E., Khutoryanskiy, V.V., “Biomedical applications of hydrogels: A review of patents and commercial products”, Eur. Polym. J., 2015.
3. Peppas, N.A., Bures, P., Leobandung, W., et al., “Hydrogels in pharmaceutical formulations”, Eur. J. Pharm. Biopharm., 2000.
4. Zhang, Y., Zhao, X., “Natural polymer-based hydrogels for drug delivery and tissue engineering”, J. Mater. Chem. B, 2020.
5. Wang, H., Li, J., Chen, F., “Stimuli-responsive hydrogels: from basic research to clinical applications”, Acta Biomater., 2018.
6. Lee, K.Y., Mooney, D.J., “Hydrogels for drug delivery and tissue engineering”, Chem. Rev., 2012.
7. Zhu, L.W., Wang, J.Y., Bai, D., “Application value of nano-composite methacrylated gelatin hydrogels in different bone defect environments”, Chin. J. Tissue Eng. Res., 2024.
8. Liu, X.Y., Liao, Y., Li, J.R., et al., “Self-regulating hydrogel for diabetic wound healing: From animal models to a pilot clinical study”, Sci. Adv., 2026.
9. Xu, X., Zhang, H., “Nanohydrogels for targeted drug delivery: Design, preparation and applications”, J. Control. Release, 2019.
10. Chen, J., Wang, L., “3D printed hydrogels for tissue engineering and regenerative medicine”, Biomacromolecules, 2021.




 齐岳微信公众号
齐岳微信公众号 官方微信
官方微信 库存查询
库存查询