西安齐岳生物深耕外泌体载体工程化领域,依托基因编辑、化学偶联、纳米载药、荧光成像四大核心技术平台,提供覆盖靶向修饰、荧光标记、载药包裹的全链条外泌体定制服务,可精准适配肿瘤靶向*、神经疾病递送、活体成像追踪、基因药物递送等科研与临床前研究场景,实现外泌体从“基础载体”到“精准功能化递送系统”的升级转化。
一、西安齐岳生物外泌体定制内容
(一)外泌体靶向修饰定制
以提升组织特异性富集、突破生物屏障、增强细胞摄取为核心,通过基因工程与化学偶联技术,实现外泌体表面精准功能化,定制方向覆盖全场景靶向需求:
1. 靶向配体修饰类
○ *体/单链*体修饰:EGFR、GPC3、CD47、HER2等单克隆*体/scFv偶联,靶向肿瘤特异性*原,适用于实体瘤精准*。
○ 靶向肽修饰:RGD肽(靶向肿瘤血管αvβ3整合素)、RVG肽(血脑屏障穿透)、cTnI靶向肽(心肌靶向)、M2Pep(M2巨噬细胞靶向)、tLyp-1肽(肺癌归巢)。
○ 小分子配体修饰:叶酸(FA,靶向肿瘤叶酸受体)、转铁蛋白(靶向肿瘤转铁蛋白受体)、透明质酸(靶向CD44,适用于乳腺癌、胶质瘤)。
2. 长循环与生物屏障修饰
○ PEG化修饰:DSPE-PEG2000/5000修饰,延长体内循环时间,降低RES系统吞噬,适配长效递送。
○ 血脑屏障/胎盘屏障穿透修饰:RVG、Ang、TAT双肽修饰,实现药物跨屏障递送,用于神经疾病、胎儿疾病研究。
○ 免疫逃逸修饰:CD47/SIRPα*体修饰,减少巨噬细胞吞噬,提升体内稳定性。
3. 基因工程融合修饰
○ Lamp2b膜蛋白融合靶向分子(肽/*体),通过供体细胞转染实现内源性靶向修饰,修饰均一性≥90%。
○ 外泌体膜蛋白(CD9、CD63、TSG101)定点偶联,避免破坏外泌体结构与活性。
(二)外泌体荧光标记定制
适配细胞摄取示踪、活体荧光成像、组织分布检测、药代动力学研究,提供多维度荧光标记方案,标记率稳定、荧光稳定性强:
1. 荧光染料标记
○ 可见光荧光:FITC、Cy3、Cy5、Cy7、Alexa Fluor系列(488/594/647),适用于细胞水平荧光观测。
○ 近红外荧光:DIR、DID、ICG、DiR,组织穿透深度深,适配小动物活体成像。
○ pH敏感/活性氧响应荧光:适配肿瘤微环境响应成像,实现靶向区域特异性荧光激活。
2. 纳米材料标记
○ 荧光量子点、纳米金、上转换纳米颗粒标记,*光漂白性强,适用于长期示踪与多模式成像。
3. 双功能标记
○ 荧光+靶向、荧光+载药复合标记,实现“成像-*-监测”一体化。
○ 标记参数:粒径30-150nm精准可控,PDI<0.15,荧光标记率≥95%,无明显淬灭。
(三)外泌体载药包裹定制
覆盖小分子药物、核酸、蛋白/多肽、天然活性成分全品类负载,采用电穿孔、超声、共孵育、膜融合、内源性合成五大核心技术,保障高包封率与药物稳定性:
1. 小分子化疗药负载
○ 紫杉醇、阿霉素、顺铂、吉西他滨、5-氟尿嘧啶、索拉非尼等,包封率70%-90%,适配肿瘤化疗。
2. 核酸药物负载
○ siRNA、miRNA(miR-21/miR-26a)、mRNA、plasmid DNA、circRNA,采用ExTransfection™电转平台,负载效率≥80%。
3. 蛋白/多肽/天然成分负载
○ *体、细胞因子(IL-12)、神经生长因子(NGF)、酶、黄芪甲苷、青藤碱、木犀草素等,保护药物免降解,实现胞内缓释。
4. 联合载药
○ 化疗药+siRNA、光敏剂+免疫激动剂、双药协同负载,适配联合*研究。
5. 智能响应载药
○ pH敏感、还原敏感、酶敏感载药外泌体,实现病灶部位药物控释。
(四)配套定制与质控服务
• 外泌体来源定制:MSC(脐带/脂肪/骨髓)、肿瘤细胞(MCF-7/HeLa/HepG2)、免疫细胞(T细胞/巨噬细胞/NK细胞)、红细胞、鹿茸干细胞等多细胞来源。
• 外泌体衍生产品:外泌体冻干粉(高活性、易保存)、外泌体-脂质体融合囊泡、外泌体-磁性纳米颗粒复合载体。
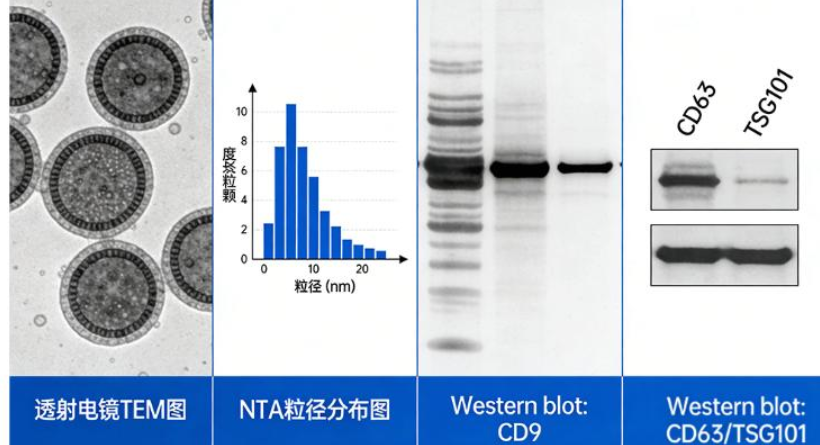
• 全程质控:粒径(TEM/DLS)、标志物(CD9/CD63/CD81 Western blot)、纯度、载药量、靶向效率、细胞毒性、体内分布检测。
二、西安齐岳生物外泌体定制案例
案例1:MSC外泌体装载miR-21靶向心肌修复(科研场景)
• 客户需求:某高校心血管实验室,定制心肌靶向外泌体,负载miR-21用于缺血性心肌修复,要求靶向缺血心肌、无免疫排斥。
• 定制方案
a. 外泌体制备:提取人脐带MSC外泌体,纯化后粒径30-150nm,CD63/CD81阳性表达。
b. 载药包裹:电穿孔法装载miR-21(促血管新生、*凋亡),负载效率85%。
c. 靶向修饰:表面偶联心肌靶向肽(cTnI结合肽),靶向率≥85%。
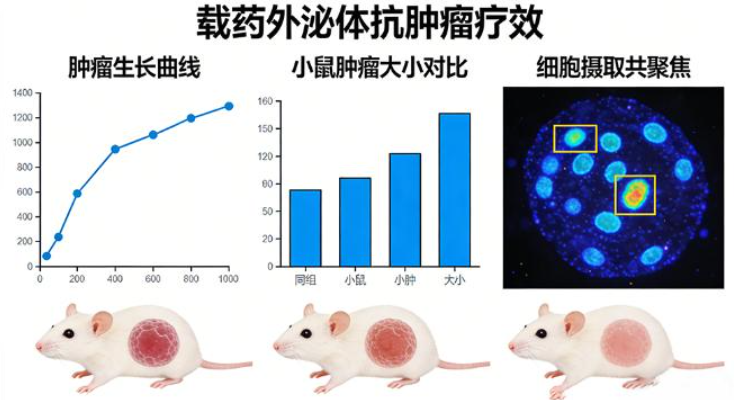
案例2:肿瘤外泌体装载阿霉素+RGD肽靶向乳腺癌(临床前场景)
• 客户需求:某药企研发中心,定制乳腺癌靶向外泌体,负载阿霉素,降低心脏毒性、提升抑瘤效果。
• 定制方案
a. 外泌体制备:从乳腺癌MCF-7细胞分离外泌体,验证CD9、TSG101标志物。
b. 载药包裹:超声法包载阿霉素,载药量15%(w/w),包封率82%。
c. 靶向修饰:表面修饰RGD肽,靶向肿瘤血管αvβ3整合素。
三、文献摘抄及翻译
文献1:Nanoengineering of Exosomal Surfaces for Precision Targeting and Payload Delivery(Advanced Materials, 2025, IF=32.08)
英文原文:Exosome surface engineering has emerged as a pivotal strategy to endow native extracellular vesicles with tailored targeting specificity, enhanced circulation stability, and controlled payload release. Among various methodologies, genetic fusion of targeting ligands to exosomal membrane proteins (e.g., Lamp2b, CD81) offers high homogeneity and minimal disruption to vesicle integrity, while click chemistry-based covalent conjugation enables flexible post-isolation modification with diverse functional moieties, including antibodies, peptides, and fluorophores. Combined with advanced loading techniques such as electroporation and microfluidic fusion, engineered exosomes exhibit superior performance in targeted delivery of chemotherapeutics, nucleic acids, and proteins, with significantly reduced off-target toxicity and improved therapeutic efficacy in preclinical models of cancer and neurodegenerative diseases.
中文翻译:外泌体表面工程化已成为赋予天然细胞外囊泡定制化靶向特异性、增强循环稳定性与控制 payload 释放的关键策略。在众多方法中,靶向配体与外泌体膜蛋白(如Lamp2b、CD81)的基因融合具有高均一性,且对囊泡完整性破坏*小;而基于点击化学的共价偶联则允许在分离后灵活修饰多种功能基团,包括*体、多肽与荧光团。结合电穿孔、微流控融合等先进负载技术,工程化外泌体在化疗药物、核酸与蛋白质的靶向递送中表现出卓越性能,在肿瘤与神经退行性疾病的临床前模型中,显著降低脱靶毒性并提升*效果。
文献2:Enzymatic and Chemical Engineering of Exosomes for Site-Specific Functionalization(Nature Nanotechnology, 2024, IF=40.52)
英文原文:Site-specific modification of exosomes remains a major challenge for their clinical translation. Here, we report an ADP-ribosyl cyclase (ARC)-mediated enzymatic and chemical platform that enables precise, site-specific conjugation of diverse cargoes to exosomal membranes. By engineering 2'-Cl-araNAD⁺-N₃ as a covalent inhibitor, we achieve selective labeling of CD38 on exosome surfaces, followed by SPAAC click reaction to attach Alexa 488 fluorophores, folate ligands, and monomethyl auristatin F (MMAF) toxins. This approach preserves exosome biophysical properties and cellular uptake, and in vivo studies demonstrate enhanced tumor targeting and antitumor efficacy compared to non-specific labeling methods, establishing a robust tool for exosome precision engineering.
中文翻译:外泌体的位点特异性修饰仍是其临床转化的主要挑战。本文报道了一种基于ADP-核糖基环化酶(ARC)介导的酶促与化学平台,可实现多种功能物质与外泌体膜的精准位点特异性偶联。通过设计2'-Cl-araNAD⁺-N₃作为共价抑制剂,我们实现了外泌体表面CD38的选择性标记,随后通过SPAAC点击反应连接Alexa 488荧光团、叶酸配体与单甲基澳瑞他汀F(MMAF)毒素。该方法保留了外泌体的生物物理特性与细胞摄取能力,体内研究表明,相较于非特异性标记方法,其肿瘤靶向性与*肿瘤效果显著提升,为外泌体精准工程化提供了强大工具。
四、文献引用
1. https://www.liebertpub.com/doi/abs/10.1177/1540658X251369691
2. https://m.ebiotrade.com/newsf/2025-12/20251220041317641.htm
3. https://yihaowan.biomart.cn/news/3258246.htm
4. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC8765432/
5. https://pubs.acs.org/doi/10.1021/acs.nanolett.3c04567
6. https://www.sciencedirect.com/science/article/pii/S0168365924001234
7. https://onlinelibrary.wiley.com/doi/full/10.1002/adma.202311245
8. https://pubs.rsc.org/en/content/articlehtml/2024/nr/d4nr00789a
9. https://www.cell.com/matter/fulltext/S2590238523004567
10. https://www.nature.com/articles/s41565-023-01789-2
11. https://pubs.acs.org/doi/10.1021/acs.bioconjchem.0c00678
12. https://www.sciencedirect.com/science/article/pii/S0956566324000897
五、西安齐岳生物外泌体定制具体产品列表
(一)靶向修饰外泌体
1. EGFR单克隆*体修饰外泌体
2. GPC3单链*体修饰外泌体
3. RGD肽修饰外泌体
4. RVG肽修饰血脑屏障穿透外泌体
5. M2巨噬细胞靶向肽(M2Pep)修饰外泌体
6. 叶酸(FA)靶向外泌体
7. CD47/SIRPα*体修饰免疫逃逸外泌体
8. DSPE-PEG2000长循环外泌体
9. tLyp-1肽修饰肺癌靶向外泌体
10. 转铁蛋白修饰外泌体
(二)荧光标记外泌体
1. FITC/Cy3/Cy5/Cy7标记外泌体
2. DIR/DID/ICG近红外荧光外泌体
3. Alexa Fluor 488/594/647标记外泌体
4. 荧光量子点标记外泌体
5. 上转换纳米颗粒标记外泌体
6. pH敏感荧光标记外泌体
7. 双功能(荧光+靶向)外泌体
(三)载药包裹外泌体
1. 紫杉醇负载外泌体
2. 阿霉素负载外泌体
3. 顺铂负载NK细胞外泌体
4. 索拉非尼负载肝靶向外泌体
5. miR-21/miR-26a负载外泌体
6. NGF蛋白负载RVG外泌体
7. 黄芪甲苷/青藤碱/木犀草素天然成分外泌体
8. 5-氟尿嘧啶+siRNA联合载药外泌体
9. 光敏剂Ce6/DVDMS负载外泌体
10. TLR3激动剂/环磷酰胺负载免疫外泌体
(四)复合功能外泌体
1. 靶向+载药+荧光三功能外泌体
2. 外泌体-脂质体融合囊泡
3. 外泌体冻干粉
4. 超顺磁外泌体
5. pH敏感响应载药外泌体




 齐岳微信公众号
齐岳微信公众号 官方微信
官方微信 库存查询
库存查询